题目内容
右表是元素周期表中短周期的一部分,已知A元素的原子中最外层电子数是其电子层数的3倍。下列关于表中六祌元素的说法不正确的是
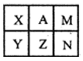

| A. X元素形成的气态氢化物分子空间结构呈三角锥形 |
| B. X、Y、Z三种元素形成的单核阴离子半径中Y最大 |
| C.X的氢化物分子间存在氢键,因此X的熔沸点较高 |
| D.最高价氧化物对应的水化物酸性最强的元素是M元素 |
D
A元素的原子中最外层电子数是其电子层数的3倍,即A为O元素,X为N元素,M为F元素,N为CL元素,Z为S元素,Y为P元素;所以
A正确,X元素形成的气态氢化物分子为NH3,分子空间结构呈三角锥形;B正确,X、Y、Z三种元素形成的单核阴离子分别为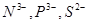 ,半径最大的为
,半径最大的为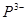 ;C正确,X的氢化物为H2O,分子间存在氢键,所以熔沸点较高;D错,最高价氧化物对应的水化物酸性最强即元素的非金属性最强,应为N即CL元素;因为F元素无最高价;
;C正确,X的氢化物为H2O,分子间存在氢键,所以熔沸点较高;D错,最高价氧化物对应的水化物酸性最强即元素的非金属性最强,应为N即CL元素;因为F元素无最高价;
A正确,X元素形成的气态氢化物分子为NH3,分子空间结构呈三角锥形;B正确,X、Y、Z三种元素形成的单核阴离子分别为
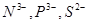 ,半径最大的为
,半径最大的为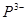 ;C正确,X的氢化物为H2O,分子间存在氢键,所以熔沸点较高;D错,最高价氧化物对应的水化物酸性最强即元素的非金属性最强,应为N即CL元素;因为F元素无最高价;
;C正确,X的氢化物为H2O,分子间存在氢键,所以熔沸点较高;D错,最高价氧化物对应的水化物酸性最强即元素的非金属性最强,应为N即CL元素;因为F元素无最高价;
练习册系列答案
相关题目
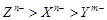
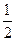 O2(g)= XO2(g) △H =" -283.0" kJ·mol-1
O2(g)= XO2(g) △H =" -283.0" kJ·mol-1