题目内容
【题目】有X、Y、Z三种元素,X原子核内无中子,Y原子的核外有三层电子层,单质在常温常压下是黄绿色气体,Z原子在反应中容易失去一个电子形成稳定的结构,和氖具有相同的电子数.按要求回答下列问题:
(1)依次写出X、Z的元素符号:、 , 画出Y原子结构示意图: .
(2)元素X、Z形成的化合物与水反应有无色气体产生,反应后的溶液能使酚酞试液变红色,请写出该反应的化学方程式 .
【答案】
(1)H,Na,
(2)H2O+NaH=NaOH+H2↑
【解析】解:有X、Y、Z三种元素,X原子核内无中子,则X为H元素;Y原子的核外有三层电子层,单质在常温常压下是黄绿色气体,则Y为Cl;Z原子在反应中容易失去一个电子形成稳定的结构,和氖具有相同的电子数,则Z为Na.(1)由上述分析可知,X为H元素、Z为Na,Y为Cl,原子结构示意图为:  ;
;
(2)元素X、Z形成的化合物为NaH,与水反应有无色气体产生,反应后的溶液能使酚酞试液变红色,反应生成NaOH与氢气,该反应的化学方程式为:H2O+NaH=NaOH+H2↑;
所以答案是:(1)H;Na;  ;(2)H2O+NaH=NaOH+H2↑
;(2)H2O+NaH=NaOH+H2↑

练习册系列答案
相关题目
【题目】如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.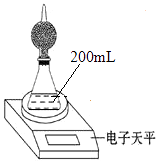
装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4molL﹣1 . 不同时间电子天平的读数如下表所示:
实验操作 | t/min | 电子天平的读数/g |
装置+硫酸溶液 | 320.0 | |
装置+硫酸溶液+样品 | 0 | 335.0 |
1 | 334.5 | |
2 | 334.1 | |
3 | 333.8 | |
4 | 333.8 |
①反应中生成气体的质量为 .
②试计算样品中铝的质量分数?(写出计算过程)
③求反应后锥形瓶内硫酸溶液(溶液的体积变化忽略)的物质的量的浓度?(写出计算过程)