题目内容
【题目】某课外活动小组用如图1装置进行实验,试回答下列问题. 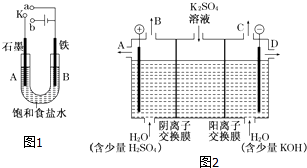
(1)若开始时开关K与a连接,则B极的电极反应式为 .
(2)若开始时开关K与b连接,则B极的电极反应式为 , 有关上述实验,下列说法正确的是(填序号) . ①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润的KI淀粉试纸变蓝
③反应一段时间后通入适量HCl可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24L气体,则溶液中转移0.1mol电子
(3)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,那么可以设想用如图2装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾. ①该电解槽的阳极反应式为 . 此时通过阴离子交换膜的离子数(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数.
②制得的氢氧化钾溶液从出口(填写“A”、“B”、“C”或“D”)导出.
③若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为 .
【答案】
(1)Fe﹣2e﹣═Fe2+
(2)2H++2e﹣═H2↑;②③
(3)4OH﹣﹣4e﹣═2H2O+O2↑;小于;D;O2+2H2O+4e﹣═4OH﹣
【解析】解:(1)开始时开关K与a连接,是原电池,铁为负极,发生氧化反应,失去电子生成亚铁离子,电极方程式为Fe﹣2e﹣═Fe2+ , 所以答案是:Fe﹣2e﹣═Fe2+;(2)开关K与b连接,装置为电解池,铁为阴极,发生还原反应,氢离子得到电子生成氢气,电极方程式为2H++2e﹣=H2↑,
所以答案是:2H++2e﹣=H2↑;①电解过程中阳离子向阴极移动,B为阴极,溶液中Na+向,B极移动,故①错误;②A生成氯气,能使湿润KI淀粉试纸变蓝,故②正确;③反应一段时间后加适量HCl气体,可恢复到电解前电解质的浓度,故③正确;④电子只能通过导线,不能通过溶液,故④错误;
所以答案是:②③;(3)①电解时,阳极上失电子发生氧化反应,溶液中的氢氧根离子的放电能力大于硫酸根离子的放电能力,所以阳极上氢氧根离子失电子生成水和氧气4OH﹣﹣4e﹣=2H2O+O2↑;阳极氢氧根离子放电,因此硫酸根离子向阳极移动,阴极氢离子放电,因此钠离子向阴极移动,所以通过相同电量时,通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数,
所以答案是:4OH﹣﹣4e﹣=2H2O+O2↑;小于;
②阴极氢离子放电,氢氧根离子浓度增大,钾离子向阴极移动,所以氢氧化钾在阴极生成,所以答案是:D;
③燃料电池正极氧气得到电子,与水生成氢氧根,电极方程式为O2+2H2O+4e﹣=4OH﹣ , 所以答案是:O2+2H2O+4e﹣=4OH﹣ .

【题目】按要求写出方程式.
(1)碳酸氢铵溶液中加入过NaOH溶液,并加热(写出离子方量程式) .
(2)已知4℃时四种化合物在水中和液氨中的溶解度如表:
AgNO3 | Ba(NO3)2 | AgCl | BaC12 | |
H2O (液) | 170g | 9.2g | 1.5×10﹣4g | 33.3g |
NH3(液) | 86g | 97.2g | 0.8g | 0g |
上述四种物质在水中形成复分解反应的离子方程式为 , 在液氨中发生复分解反应的化学方程式为 .
【题目】下列实验能达到相应目的是( )
选项 | A | B | C | D |
实验过程 |
|
|
|
|
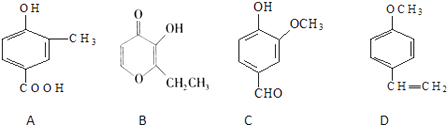
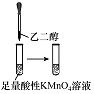
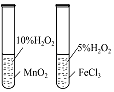
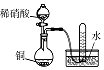
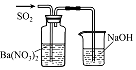
实验目的 | 将乙二醇(HOCH2CH2OH)转化为乙二酸(H2C2O4) | 比较氯化铁和二氧化锰对H2O2分解反应的催化效果 | 证明稀硝酸与铜反应时表现出氧化性 | 用SO2与Ba(NO3)2反应获得BaSO3沉淀 |
A.A
B.B
C.C
D.D