题目内容
某化学学习小组学习电化学后,设计了下面的实验装置图: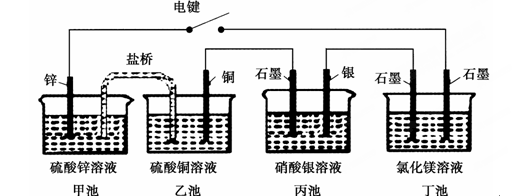
下列有关该装置图的说法中正确的是( )
| A.合上电键后,盐桥中的阳离子向甲池移动 |
| B.合上电键后,丙池为电镀银的电镀池 |
| C.合上电键后一段时间,丙池中溶液的pH增大 |
| D.合上电键后一段时间,当丙池中生成标准状况下560 mL气体时,丁池中理论上最多产生2.9 g固体 |
D
解析试题分析:合上电键后,甲池和乙池构成原电池,丙池、丁池分别形成电解池。A、锌的活泼性大于铜,所以锌为原电池的负极,铜为正极,盐桥中的阳离子向正极移动,即向甲池移动,错误;B、丙池中石墨为阳极,银为阴极,电解硝酸银溶液生成HNO3、Ag和O2,不是电镀池,错误;C、合上电键后一段时间,丙池中生成HNO3、Ag和O2,溶液的pH降低,错误;D、根据化合价的变化可得对应关系式:O2 ~ 2Mg(OH)2所以当丙池中生成标准状况下560 mL气体时,丁池中理论上最多产生的固体质量为:0.56L÷22.4L/mol×2×58g/mol=2.9g,正确。
考点:本题考查原电池与电解池原理及应用。

练习册系列答案
相关题目
下列叙述错误的是( )
| A.废弃的干电池不能随意丢弃,但可以土埋处理 |
| B.马口铁(镀锡铁)镀层破损后即失去保护作用 |
| C.不能将铁制自来水管与铜制水龙头连接使用 |
| D.电化学腐蚀过程中存在电极反应,产生微电流 |
在理论上不能用于设计原电池的化学反应是
| A.2FeCl3(aq)+2KI(aq) = 2FeCl2(aq)+2KCl(aq)+I2(aq) △H <0 |
| B.Ba(OH)2·8H2O(s)+2NH4Cl(s) = BaCl2(aq)+2NH3·H2O(aq)+8H2O(1) △H >0 |
| C.4Al(s)+ 6H2O(1)+ 3O2(g)==4Al(OH)3(s) △H <0 |
| D.Zn(s)+2MnO2(s)+2H2O(1) = 2MnOOH(s) +Zn(OH)2(s) △H <0 |
随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到570℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质,用吸附在它内外表面上的金属钯多晶薄膜做电极,实现了常压、570℃条件下高转化率的电解法合成氨(装置如图)。下列有关说法中正确的是 
| A.电解法合成氨的电解池中能用水作电解质溶液的溶剂 |
| B.钯电极B连接的是电源的负极 |
| C.钯电极A的电极反应式为:N2+6e—+6H+==2NH3 |
| D.当有0.3mol电子转移时,有2.688L NH3生成 |
如图所示,下列叙述中正确的是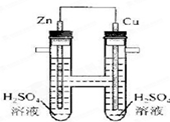
| A.正极发生氧化反应 | B.电子通过导线由铜流向锌 |
| C.负极有O2逸出 | D.铜上有H2逸出 |
蓄电池在放电时起原电池作用,在充电时起电解池作用。下面是爱迪生蓄电池分别在充电和放电时发生的反应:Fe+NiO2+2H2O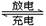 Fe(OH)2+Ni(OH)2。下列有关爱迪生蓄电池的说法正确的是
Fe(OH)2+Ni(OH)2。下列有关爱迪生蓄电池的说法正确的是
| A.放电时,Fe是负极,发生还原反应,NiO2是正极,发生氧化反应 |
| B.蓄电池的电极可以浸入某种酸性电解质溶液中 |
| C.放电时,电解质溶液中的阴离子向正极方向移动 |
| D.充电时,阴极上的电极反应式为:Fe(OH)2+2e-=Fe+2OH- |
下列事实与电化学腐蚀无关的是
| A.生铁比纯铁易生锈 |
| B.黄铜(铜锌合金)制品不易产生铜绿 |
| C.纯银饰品久置表面变暗 |
| D.与铜管连接的铁管易生锈 |
下列叙述正确的是
| A.电解饱和食盐水制烧碱采用离子交换膜法,可以阻止阳离子通过 |
| B.在铁上镀锌时,锌棒作阴极,且电解液硫酸锌的浓度是不变的 |
| C.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1: 2 |
| D.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 molNaOH |