题目内容
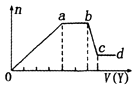
【题目】某无色稀溶液X中,可能含有如表所列离子中的某几种.取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(y)的关系如图所示.下列说法正确的是( )
阴离子 | CO32﹣、SiO32﹣、[Al(OH)4]﹣、Cl﹣ |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
A.若Y是盐酸,则X中一定含有CO32﹣、SiO32﹣、[Al(OH)4]﹣和NH4+
B.若Y是NaOH溶液,则X中一定含有A13+、Fe3+、NH4+、Cl﹣
C.若Y是NaOH溶液,则ab段发生反应的离子方程式为:NH4++OH﹣═NH3↑+H2O
D.若Y是NaOH溶液,则X中的Al3+、Mg2+、NH4+物质的量之比为2:1:4
【答案】D
【解析】解:溶液无色说明溶液中不含Fe3+;(1)如果Y是盐酸,向溶液中加盐酸,先生成沉淀,则溶液中可能含SiO32﹣、[Al(OH)4]﹣或两者中的一种,即生成的沉淀为H2SiO3、Al(OH)3或两者中的一种,则溶液中不含Al3+、Mg2+;当a﹣b段时,沉淀的量不变化,发生的是盐酸和碳酸根离子反应生成气体:CO32﹣+H+═HCO3﹣ , HCO3﹣+H+═H2O+CO2↑;当b﹣c段时沉淀的质量减少,即部分沉淀和盐酸反应:Al(OH)3+3H+═Al3++3H2O,部分沉淀和盐酸不反应,说明生成的沉淀既有H2SiO3又有Al(OH)3 , 原溶液中有SiO32﹣和[Al(OH)4]﹣ , 则oa段发生反应的离子方程式SiO32﹣+2H+═H2SiO3↓,[Al(OH)4]﹣+H+═Al(OH)3↓+H2O,由于SiO32﹣和[Al(OH)4]﹣和铵根离子能双水解,所以溶液中不含NH4+ , 含有的阳离子是Na+ . 则X中一定含有的离子是CO32﹣、SiO32﹣、AlO2﹣、Na+ , oa段发生反应的离子方程式SiO32﹣+2H+═H2SiO3↓,[Al(OH)4]﹣+H+═Al(OH)3↓+H2O,ab段发生反应的离子方程式CO32﹣+H+═HCO3﹣ , HCO3﹣+H+═H2O+CO2↑,bc段发生反应的离子方程式:Al(OH)3+3H+═Al3++3H2O.
综上可知含有的离子为:CO32﹣、SiO32﹣、AlO2﹣、Na+;(2)若Y是氢氧化钠,向溶液中加氢氧化钠溶液,先生成沉淀,溶液中可能含Al3+、Mg2+或两者中的一种,由于弱碱阳离子和弱酸根会双水解而不能共存,即溶液中不含CO32﹣、SiO32﹣、[Al(OH)4]﹣ , 由于溶液一定要保持电中性,故溶液中一定含Cl﹣;当a﹣b段时,沉淀的量不变化,是氢氧化钠和铵根离子反应生成气体:NH4++OH﹣═NH3H2O,即溶液中含NH4+;当b﹣c段时沉淀的质量减少但没有完全溶解,即部分沉淀和氢氧化钠反应,部分沉淀不反应,说明溶液中有Al3+、Mg2+ , 即bc段的反应为:Al(OH)3+OH﹣═AlO2﹣+2H2O.
综上可知,X中一定含有的离子是Al3+、Mg2+、NH4+、Cl﹣;
A.由分析可知,若Y是盐酸,则X中一定含有:CO32﹣、SiO32﹣、AlO2﹣、Na+ , 故A错误;
B.若Y是氢氧化钠,X中一定含有的离子是Al3+、Mg2+、NH4+、Cl﹣ , 没有Fe3+ , 故B错误;
C.若Y是NaOH溶液,当a﹣b段时,沉淀的量不变化,是氢氧化钠和铵根离子反应生成气体:NH4++OH﹣═NH3H2O,故C错误;
D.与铵根离子反应需要氢氧化钠的体积是2v,氢氧化铝和氢氧化钠反应需要氢氧化钠的体积是1v,则生成氢氧化铝需要氢氧化钠的体积是3V,生成氢氧化镁需要氢氧化钠的体积是1V,则n(Al3+):n(Mg2+):n(NH4+)=1: ![]() :2=2:1:4,故D正确.
:2=2:1:4,故D正确.
故选D.