题目内容
【题目】在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A.SiO2 ![]() SiCl4
SiCl4 ![]() Si
Si
B.FeS2 ![]() SO2
SO2 ![]() H2SO4
H2SO4
C.N2 ![]() NH3
NH3 ![]() NH4Cl(aq)
NH4Cl(aq)
D.MgCO3 ![]() MgCl2(aq)
MgCl2(aq) ![]() Mg
Mg
【答案】C
【解析】解:A.二氧化硅属于酸性氧化物和盐酸不反应,不能一步实现反应,故A错误;
B.二氧化硫和水反应生成亚硫酸,亚硫酸被氧化生成硫酸,二氧化硫和水不能一步转化,故B错误;
C.氮气和氢气在催化剂、高温高压条件下反应生成氨气,氨气是碱性气体和盐酸反应生成氯化铵,两步反应能一步实现,故C正确;
D.碳酸镁溶于盐酸生成氯化镁溶液,氯化镁溶液电解得到氢氧化镁,氢气和氯气,不能直接得到金属镁,应是电解熔融状态的氯化镁得到金属镁,故D错误;
故选C.
A.二氧化硅为酸性氧化物和盐酸不反应;
B.FeS2燃烧生成二氧化硫,二氧化硫和水反应生成亚硫酸;
C.氮气和氢气一定条件下反应生成氨气,氨气和盐酸反应生成氯化铵;
D.碳酸镁和盐酸反应生成氯化镁、二氧化碳和水,氯化镁溶液电解不能生成金属镁.

【题目】等质量的 SO2和 SO3相比较,下列结论正确的是( )
A. 它们的分子数目之比是 4:5
B. 它们的氧元素的质量之比为 2:3
C. 它们的物质的量之比为 5:4
D. 它们的密度之比为 5:4
【题目】某无色稀溶液X中,可能含有如表所列离子中的某几种.取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(y)的关系如图所示.下列说法正确的是( )
阴离子 | CO32﹣、SiO32﹣、[Al(OH)4]﹣、Cl﹣ |
阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
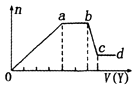
A.若Y是盐酸,则X中一定含有CO32﹣、SiO32﹣、[Al(OH)4]﹣和NH4+
B.若Y是NaOH溶液,则X中一定含有A13+、Fe3+、NH4+、Cl﹣
C.若Y是NaOH溶液,则ab段发生反应的离子方程式为:NH4++OH﹣═NH3↑+H2O
D.若Y是NaOH溶液,则X中的Al3+、Mg2+、NH4+物质的量之比为2:1:4