题目内容
【题目】向1L浓度均为![]() 和氢氧化钠的混合溶液中缓慢加入二氧化碳,随
和氢氧化钠的混合溶液中缓慢加入二氧化碳,随![]() 增大,溶液中下列离子浓度对应关系正确的是 ( )
增大,溶液中下列离子浓度对应关系正确的是 ( )
选项 |
| 溶液中离子的物质的量浓度关系 |
A |
| c(Na+)>c(CO32-)>c(OH-)>c(AlO2-) |
B |
|
|
C |
|
|
D |
|
|
A.AB.BC.CD.D
【答案】B
【解析】
n(NaOH)=n(NaAlO2)=0.1mol/L×1L=0.1mol,随着CO2的通入依次发生的反应为CO2+2NaOH=Na2CO3+H2O、CO2+2NaAlO2+3H2O=2Al(OH)3↓+Na2CO3、CO2+Na2CO3+H2O=2NaHCO3;
![]() 当
当![]() 时,
时,![]() 氢氧化钠消耗
氢氧化钠消耗![]() 二氧化碳,生成
二氧化碳,生成![]() 碳酸钠,所得溶液中溶质为
碳酸钠,所得溶液中溶质为![]() 碳酸钠和
碳酸钠和![]() 偏铝酸钠,所以
偏铝酸钠,所以![]() ,正确的离子浓度大小为:
,正确的离子浓度大小为:![]() ,选项A错误;
,选项A错误;
B、当![]() 时,所得溶液中溶质为
时,所得溶液中溶质为![]() 碳酸钠,溶液中的物料守恒为
碳酸钠,溶液中的物料守恒为![]() ,所以
,所以![]() ,选项B正确;
,选项B正确;
C.当![]() 时,即在B的基础上再通
时,即在B的基础上再通![]() ,所得溶液中溶质为
,所得溶液中溶质为![]() 碳酸钠和
碳酸钠和![]() 碳酸氢钠,则
碳酸氢钠,则![]() 最小,正确的离子浓度的关系为:
最小,正确的离子浓度的关系为:![]() ,选项C错误;
,选项C错误;
D.当![]() 时,所得溶液中溶质为
时,所得溶液中溶质为![]() 的碳酸氢钠,溶液中的电荷守恒为
的碳酸氢钠,溶液中的电荷守恒为![]() ,选项D错误;
,选项D错误;
答案选B。

【题目】煤化工中常需研究不同温度下平衡常数、投料比及产率等问题。已知:CO(g)+H2O(g)![]() CO2(g)+H2(g)的平衡常数随温度的变化如下表:下列叙述正确的是
CO2(g)+H2(g)的平衡常数随温度的变化如下表:下列叙述正确的是
温度/℃ | 400 | 500 | 830 | 1000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
A. 该反应的正反应是吸热反应
B. 该反应达到平衡后,保持容器休积不变升高温度,正反应速率不变,容器内混合气体的压强不变
C. 830℃时,在恒容反应器中按物质的量比n(CO):n(H2O):n(H2):n(CO2)=2:4:6:1投入反应混合物发生上述反应,初始时刻v正<v逆
D. 830℃时,在2L的密闭容器中加入4molCO(g)和6molH2O(g)达到平衡时,CO的转化率是60%
【题目】结合下表回答下列问题:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
溶度积/25 ℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
现有某酸性CuCl2溶液中含有少量的FeCl2,为得到纯净的CuCl2·2H2O晶体,按如图步骤进行提纯:
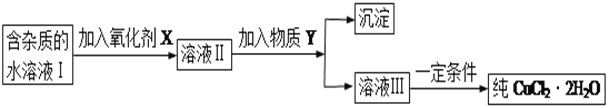
(1)最适合作氧化剂X的是_________(填字母),加入X的目的是____________________________________。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
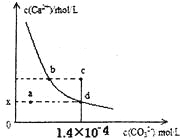
加入的物质Y是____________(填化学式),调至溶液pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=____________。过滤后,将所得滤液低温蒸发、浓缩结晶,可得到CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是______________________________________________________。
(3)含Cr2O![]() 的废水毒性较大,某工厂废水中含5.0×10-3 mol·L-1的Cr2O
的废水毒性较大,某工厂废水中含5.0×10-3 mol·L-1的Cr2O![]() ,为了使废水的排放达标,进行如下处理:
,为了使废水的排放达标,进行如下处理:
![]()
①绿矾化学式为FeSO4·7H2O,反应(I)的离子方程式为________________________________;
②若处理后的废水中c(Cr3+)=3.0×10-6 mol·L-1,则废水中c(Fe3+)= _________ mol·L-1。(Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH) 3]=6.0×10-31)