题目内容
6.过量的锌粉与一定量的稀盐酸反应,为了加快反应速率,但是又不影响生成的氢气总量,可以采取的措施是( )| A. | 适当升高温度 | B. | 加入适量的水 | ||
| C. | 加入少量CuSO4溶液 | D. | 加入浓度较大的硝酸 |
分析 过量锌与少量稀硫酸反应,为了加快反应速率,可以升高温度、增大锌固体的表面积或形成原电池反应,不影响生成氢气的总量,所加入物质不能改变氢离子的总物质的量,以此解答该题.
解答 解:A、升温,活化分子数目增多,反应速率加快,故A正确;
B、加水稀释,氢离子浓度降低,反应速率减慢,故B错误;
C、加入少量硫酸铜溶液,能够形成锌铜原电池,加快反应速率,氢离子物质的量不变,生成氢气总量不变,故C正确;
D、加入硝酸,硝酸与锌反应不生成氢气,故D错误;
故选AC.
点评 本题考查化学反应速率的影响因素,题目难度不大,易错点为D,注意硝酸与锌反应不生成氢气.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
7.最能说明镁的金属性比钙弱的事实是( )
| A. | 钙能与冷水反应,镁与热水反应 | |
| B. | 碳酸镁微溶于水,碳酸钙难溶于水 | |
| C. | 氢氧化镁难溶于水,氢氧化钙微溶于水 | |
| D. | 钙能置换氯化镁溶液中的镁 |
17.下表标出的是元素周期表的一部分元素,回答下列问题:
(1)表中用字母标出的14种元素中,化学性质最不活泼的是Ar(用元素符号表示,下同),金属性最强的是K,非金属性最强的是F常温下单质为液态的非金属元素是Br,属于过度元素的是M(该空用字母表示).
(2)B,F,C的气态氢化物中以PH3最不稳定(填化学式).
(3)除稀有气体外第三周期中原子半径最小的是Cl(填元素符号)
(4)写出I、H号元素最高价氧化物的对应水化物的化学式:Mg(OH)2和Al(OH)3.强弱顺序是Mg(OH)2>Al(OH)3.
| 1 | ||||||||||||||||||
| 2 | D | B | A | |||||||||||||||
| 3 | J | I | H | C | G | F | E | |||||||||||
| 4 | L | K | M | N | ||||||||||||||
(2)B,F,C的气态氢化物中以PH3最不稳定(填化学式).
(3)除稀有气体外第三周期中原子半径最小的是Cl(填元素符号)
(4)写出I、H号元素最高价氧化物的对应水化物的化学式:Mg(OH)2和Al(OH)3.强弱顺序是Mg(OH)2>Al(OH)3.
14.下列说法中正确的是( )
| A. | CO2、NH3、BF3中,所有原子都满足最外层8电子的稳定结构 | |
| B. | 在元素周期表中金属和非金属交界处可以找到半导体材料 | |
| C. | 由非金属元素组成的化合物一定是共价化合物 | |
| D. | 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键 |
1.最近,日本在一公园内检测到放射性物质包括碘131和铯137,引起社会恐慌.有关资料显示其中,碘131一旦被人体吸入,可能会引发甲状腺疾病,铯137则会造成人体造血系统和神经系统损伤.请问这两个原子53131I和55137Cs的核内中子数分别为( )
| A. | 53和55 | B. | 131和137 | C. | 78和82 | D. | 76和79 |
11.某有机物的结构简式为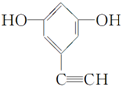 ,它的含有醛基(-CHO)的芳香族化合物的同分异构体共有( )
,它的含有醛基(-CHO)的芳香族化合物的同分异构体共有( )
 ,它的含有醛基(-CHO)的芳香族化合物的同分异构体共有( )
,它的含有醛基(-CHO)的芳香族化合物的同分异构体共有( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
18.常温时,向pH=2的硫酸中加入等体积的下列溶液后,滴入甲基橙试液,出现红色,该溶液可能是( )
| A. | pH=12 的Ba(OH)2 | B. | pH=12的氨水 | C. | 0.005mol/L NaOH | D. | 0.05mol/L BaCl2 |
15.下列各组中的反应,属于同一反应类型的是( )
| A. | 乙烯水化制乙醇;溴乙烷水解制乙醇 | |
| B. | 甲苯使酸性高锰酸钾溶液褪色;丙炔使溴的四氯化碳溶液褪色 | |
| C. | 乙醇脱水制乙烯;溴乙烷与NaOH乙醇溶液共热制乙烯 | |
| D. | 苯的硝化;苯与氢气(镍作催化剂)制取环己烷 |
16.结合学过的化学知识,判断下列叙述正确的是( )
| A. | 明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 | |
| B. | 日常生活中无水乙醇常用于杀菌消毒 | |
| C. | 丁达尔效应是区分胶体和溶液的一种常用物理方法 | |
| D. | 加铁酱油就是在酱油中加入了纳米级别的铁粉,是我国的补铁工程 |