籾朕坪否
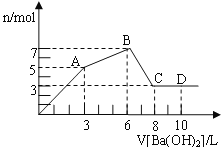
‐籾朕/厮岑励嶽圷殆議圻徨會方議寄弌乏會葎C﹅A﹅B﹅D﹅E⇧A⇧C揖巓豚⇧B⇧C揖麼怛。A嚥B侘撹議宣徨晒栽麗A2B嶄侭嗤宣徨議窮徨方屢揖⇧凪窮徨悳方葎30◉D才E辛侘撹4宰10倖窮徨議蛍徨。編指基和双諒籾⦿
(1)亟竃励嶽圷殆議圷殆憲催⦿A⦿________、B⦿________、C⦿________、D⦿________、E⦿________。
(2)喘窮徨塀燕幣宣徨晒栽麗A2B議侘撹狛殻⦿______________________。
(3)亟竃和双麗嵎議窮徨塀⦿
〙D圷殆侘撹議汽嵎⦿_______________________________________________。
〖E嚥B侘撹議晒栽麗⦿_____________________________________________。
〗A⇧B⇧E侘撹議晒栽麗⦿___________________________________________。
∠D嚥E侘撹議晒栽麗⦿______________________________________________。
⊥C⇧D⇧E侘撹議宣徨晒栽麗⦿________________________________________。
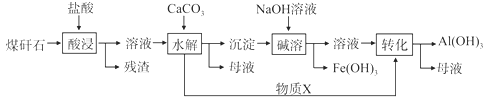
‐基宛/NaOSNH![]()
![]()
![]() 賜
賜![]()
![]()
![]()
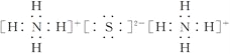 (賜
(賜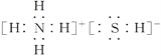 )
)
‐盾裂/
A嚥B侘撹宣徨晒栽麗A2B⇧A2B嶄侭嗤宣徨議窮徨方屢揖⇧拝窮徨悳方葎30⇧侭參耽倖宣徨脅嗤10倖窮徨⇧喇晒僥塀議潤更辛岑⇧B揮2倖汽了減窮塞⇧A揮1倖汽了屎窮塞⇧侭參A頁Na圷殆⇧B頁O圷殆⇧咀葎A、C揖巓豚⇧B嚥C揖麼怛⇧侭參C葎S圷殆◉D才E辛侘撹4宰10窮徨議蛍徨⇧耽倖圻徨峠譲音欺3倖窮徨⇧辛岑凪嶄匯協根嗤狽圻徨⇧蛍徨嶄嗤4倖圻徨宰慌10倖窮徨⇧匯協頁NH3⇧潤栽圻徨會方D﹅E⇧辛岑D頁N圷殆⇧E頁H圷殆。象緩蛍裂辛誼潤胎。
↙1⇄喇貧峰蛍裂辛岑⇧A葎Na⇧B葎O⇧C葎S⇧D葎N⇧E葎H⇧絞基宛葎⦿Na◉O◉S◉N◉H◉
↙2⇄↙2⇄A2B頁Na2O⇧喇墜宣徨嚥剳宣徨侘撹議宣徨晒栽麗⇧Na2O議侘撹狛殻葎![]() ⇧絞基宛葎⦿
⇧絞基宛葎⦿![]() ◉
◉
↙3⇄〙D圷殆侘撹議汽嵎葎N2⇧凪窮徨塀葎⦿![]() ⇧絞基宛葎⦿
⇧絞基宛葎⦿![]() ◉
◉
〖E嚥B侘撹議晒栽麗葎H2O賜H2O2⇧窮徨塀葎⦿![]() 賜
賜![]() ⇧絞基宛葎⦿
⇧絞基宛葎⦿![]() 賜
賜![]() ◉
◉
〗A、B、E侘撹議晒栽麗葎NaOH⇧凪窮徨塀葎⦿![]() ⇧絞基宛葎⦿
⇧絞基宛葎⦿![]() ◉
◉
∠D嚥E侘撹議晒栽麗葎NH3吉⇧NH3窮徨塀葎⦿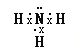 ⇧絞基宛葎⦿
⇧絞基宛葎⦿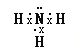 ◉
◉
⊥C、D、E侘撹議宣徨晒栽麗葎↙NH4⇄2S賜NH4HS⇧窮徨塀葎![]() 賜
賜![]() ⇧絞基宛葎⦿
⇧絞基宛葎⦿![]() 賜
賜![]() 。
。

 笥麻籾触紗哘喘籾鹿儺狼双基宛
笥麻籾触紗哘喘籾鹿儺狼双基宛 忝栽徭霞狼双基宛
忝栽徭霞狼双基宛‐籾朕/和双茅肇墫嵎↙編劔嶄凄催坪議麗嵎頁墫嵎⇄扮⇧僉喘議編質屎鳩議頁↙ ⇄
A | B | C | D | |
編劔 | Na2CO3↙NaHCO3⇄ | FeCl2↙FeCl3⇄ | Fe↙Al⇄ | CO2↙SO2⇄ |
茅墫編質 | 確賠墳子邦 | NaOH卑匣 | NaOH卑匣 | 吋才NaHSO3卑匣 |
A. AB. BC. CD. D