题目内容
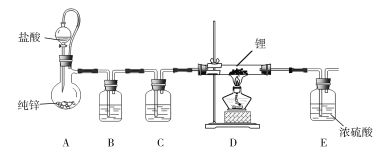
【题目】利用下图装置![]() 夹持装置略去
夹持装置略去![]() 验证CO能还原CuO并制备一定量的铜,下列说法错误的是
验证CO能还原CuO并制备一定量的铜,下列说法错误的是

A.![]() 中盛装的试剂可以是无水氯化钙
中盛装的试剂可以是无水氯化钙
B.实验中会造成环境污染
C.停止加热时首先应熄灭![]() 处酒精灯
处酒精灯
D.若![]() 中试剂减轻
中试剂减轻![]() ,则
,则![]() 中试剂会减轻
中试剂会减轻![]()
【答案】D
【解析】
A.![]() 分解产生
分解产生![]() 、
、![]() 、
、![]() ,
,![]() 在高温下与C反应转化为CO,
在高温下与C反应转化为CO,![]() 在高温下可与C反应生成
在高温下可与C反应生成![]() ,
,![]() 也能与CuO反应,干扰实验,故装置
也能与CuO反应,干扰实验,故装置![]() 可盛装干燥剂无水氯化钙干燥二氧化碳,A正确;
可盛装干燥剂无水氯化钙干燥二氧化碳,A正确;
B.尾气中的CO有毒,会污染环境,故B正确;
C.![]() 中停止加热后还应通入一段时间的气体直至其冷却,否则还原得到的铜在较高温度下可与空气中的
中停止加热后还应通入一段时间的气体直至其冷却,否则还原得到的铜在较高温度下可与空气中的![]() 反应,故C正确;
反应,故C正确;
D.由![]() 知,当有
知,当有![]() 反应时会生成
反应时会生成![]() ,若CO全部反应完,则CuO会失去
,若CO全部反应完,则CuO会失去![]() ,质量减轻
,质量减轻![]() ,但CO在
,但CO在![]() 无法全部反应完,故D错误。
无法全部反应完,故D错误。
故选D。

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】Ⅰ.一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图所示。已知达平衡后,降低温度,A的体积分数将减小。
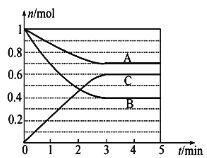
(1)该反应的化学方程式为__________。
(2)该反应的反应速率v随时间t的关系如图所示:
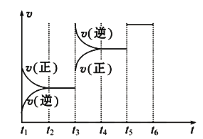
①根据上图判断,在t3时刻改变的外界条件是____________。
②A的转化率最大的一段时间是________。
③各阶段的平衡常数如下表所示:
t2~t3 | t4~t5 | t5~t6 |
K1 | K2 | K3 |
K1、K2、K3之间的大小关系为________(用“>”、“<”或“=”连接)。
Ⅱ.在密闭容器中充入一定量的H2S,发生反应2H2S(g) ![]() 2H2(g)+S2(g) ΔH,如图所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
2H2(g)+S2(g) ΔH,如图所示为H2S气体分解生成H2(g)和S2(g)的平衡转化率与温度、压强的关系。
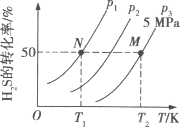
(1)△H___ (填“>”“<”或“ = ”)0。
(2)图中压强(p1、p2、p3)的大小顺序为____。
(3)图中M点的平衡常数Kp =____MPa(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)如果想进一步提高H2S的转化率,除改变温度、压强外,还可以采取的措施有___。
【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) ![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_________________________________。
(2)该反应为________反应(填“吸热”或“放热”)。
(3)某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为______。
(4)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K______1.0(填“大于”“小于”或“等于”)。
(5)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡____移动(填“向正反应方向”“向逆反应方向”或“不”)。
(6)若1 200 ℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2 mol·L-1、2 mol·L-1、4 mol·L-1、4 mol·L-1,则此时上述反应的平衡移动方向为__________(填“正反应方向”“逆反应方向”或“不移动”)。