��Ŀ����
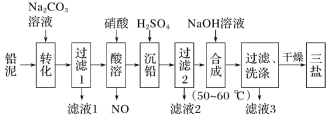
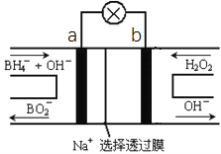
����Ŀ�����⻯��NaBH4(BԪ�صĻ��ϼ�Ϊ+3��)ȼ�ϵ��(DBFC), ���ھ���Ч�ʸߡ������������Ⱦ��ȼ�����ڴ����������ŵ㣬����Ϊ��һ�ֺ��з�չDZ����ȼ�ϵ�ء��乤��ԭ������ͼ��ʾ������˵����ȷ����
A. ��صĸ�����ӦΪBH4��+2H2O��8e��=BO2��+8H+
B. �ŵ�ʱ��ÿת��2mol���ӣ���������Ҫ����9.5gNaBH4
C. ��طŵ�ʱNa+��b��������a����
D. �缫a����MnO2��MnO2�����缫�������д�����
���𰸡�B
��������
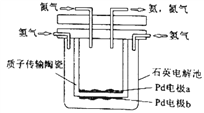
�����⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��������Һ�ʼ��ԣ��ɹ���ԭ��װ��ͼ��֪����������������Ӧ���缫��ӦʽΪBH4-+8OH--8e-=BO2-+6H2O������H2O2������ԭ��Ӧ���õ����ӱ���ԭ����OH-���缫��ӦʽΪH2O2+2e-=2OH-�����ԭ��صĹ���ԭ���ͽ�����
A����������������Ӧ����BO2-���缫��ӦʽΪBH4-+8OH--8e-=BO2-+6H2O����A����
B����������������Ӧ����BO2-���缫��ӦʽΪBH4-+8OH--8e-=BO2-+6H2O��
ÿת��2mol���ӣ���������Ҫ����0.25mol��9.5gNaBH4����B��ȷ��
C��ԭ��ع���ʱ���������������ƶ������������ƶ�����Na+��a��������b��������C����
D���缫b����MnO2��Ϊ������H2O2������ԭ��Ӧ���õ����ӱ���ԭ����OH-��MnO2�����缫�������д����ã���D����
��ѡB��

 ���ſ����ϵ�д�
���ſ����ϵ�д� ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д�����Ŀ������β���к���CO��NOx����Ⱦ���������β����Ⱦ����Ҫ�о����⡣
(1)��֪�� N2(g) + O2(g)==2NO(g) ��H=+ 180.5kJ��mol-1
2C(s)+ O2(g)== 2CO(g) ��H= - 221.0kJ��mol-1
C(s)+ O2(g)==CO2(g) ��H= -393.5 kJ��mol-1
2CO(g)+ 2NO(g)== N2(g)+ 2CO2(g) ��H=_______kJ��mol-1
(2)ij�¶��£�Ϊ̽��2CO(g)+ 2NO(g)N2(g)+ 2CO2(g)�ķ�Ӧ���ʣ������崫������ò�ͬʱ���CO��NOŨ�����±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(CO)/10-4mol��L-1 | 36.0 | 30.5 | 28.5 | 27.5 | 27.0 | 27.0 |
c(NO)/10-4mol��L-1 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
��ǰ2s�ڣ�������Ӧ��ƽ����Ӧ����v(NO)=_______��
�ڸ��¶��£�������Ӧ��ƽ�ⳣ��K=_________��
�۶���������Ӧ������������ȷ����________(����ĸ)��
A.��Ӧ�ڵ��������Է����� B.��2v��(CO)=v��(N2)ʱ����Ӧ�ﵽƽ��״̬
C.�о���Ӧ�ĸ�Ч���������ش� D.��Ӧ�ﵽƽ��ʱ��CO��NO��ת�������
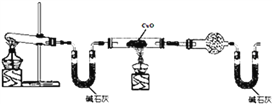
(3)COŨ�ȷ�������ȼ�ϵ��Ϊ����ԭ������װ����ͼ��ʾ���õ���е����Ϊ������-�����ƣ�����O2-�����ڹ������NASICON�������ƶ���д����缫a�ĵ缫��Ӧʽ��_________��