题目内容
【题目】席夫碱类化合物G有机合成、药物、新材料等方面有广泛应用。合成G的一种路线如下:
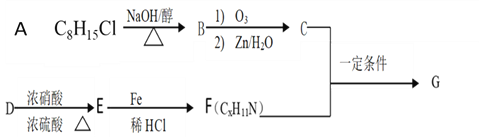
①![]()
②1molB经上述反应可生成2molC,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢
⑤![]()
回答下列问题:
(1)B的化学名称_________________,A生成B的化学方程式___________________________________
(2)A 生成B , E 生成F的反应类型分别是__________,___________
C+F 生成G的化学方程式________________________________________________________________
(3)E的同分异构体中,含有苯环和氨基且能与碳酸氢钠反应生成CO2的共有_______种,其中核磁共振氢谱有五组峰,峰面积之比为1:2:2:2:2的结构简式为________________________(任意写一种)
(4)已知![]() 请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线___________________________________________________________________________
请以乙烯为原料,其他试剂任选,写出合成吸水材料聚丙烯酸钠的合成路线___________________________________________________________________________
【答案】 3,4-二甲基-3-己烯 CH3CH2CH(CH3)-CCl(CH3)CH2CH3+NaOH![]() CH3CH2C(CH3)=C(CH3)CH2CH3+NaCl+H2O 消去反应 还原反应 CH3CH2COCH3+
CH3CH2C(CH3)=C(CH3)CH2CH3+NaCl+H2O 消去反应 还原反应 CH3CH2COCH3+![]()
![]()
![]() + H2O 17
+ H2O 17 ![]() 或
或![]() CH2= CH2
CH2= CH2![]() CH2Br CH2Br
CH2Br CH2Br![]() CH≡CH
CH≡CH![]() CH2= CHCOOCH3
CH2= CHCOOCH3![]() CH2= CHCOONa
CH2= CHCOONa![]()
![]()
【解析】A的分子式为C8H15Cl,在氢氧化钠的醇溶液、加热条件下发生消去反应得到B为烯烃,1mol B发生信息①中氧化反应生成2mol C,且C不能发生银镜反应,则B为对称结构烯烃,故B为CH3CH2C(CH3)=C(CH3)CH2 CH3,C为CH3CH2COCH3,逆推可知A为CH3CH2CH(CH3)-CCl(CH3)CH2 CH3;D属于单取代芳烃,其相对分子质量为106,D含有一个苯环,侧链式量=106-77=29,故侧链为-CH2CH3,D为![]() ;D与浓硝酸发生硝化反应生成E,E在铁和氯化氢作用下发生还原反应生成F,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为
;D与浓硝酸发生硝化反应生成E,E在铁和氯化氢作用下发生还原反应生成F,核磁共振氢谱显示F苯环上有两种化学环境的氢,故D发生乙基对位取代反应生成E为![]() ,由F的分子式可知,E中硝基被还原为-NH2,则F为
,由F的分子式可知,E中硝基被还原为-NH2,则F为![]() ,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为
,C与F发生信息⑤中反应,分子间脱去1分子水形成N=C双键得到G,则G为![]() 。
。
(1)根据上述分析,B为CH3CH2C(CH3)=C(CH3)CH2 CH3,名称为3,4-二甲基-3-己烯,A[CH3CH2CH(CH3)-CCl(CH3)CH2 CH3]发生消去反应生成B[CH3CH2C(CH3)=C(CH3)CH2 CH![]() CH3CH2C(CH3)=C(CH3)CH2 CH3+NaCl+H2O,故答案为:3,4-二甲基-3-己烯;CH3CH2CH(CH3)-CCl(CH3)CH2 CH3+NaOH
CH3CH2C(CH3)=C(CH3)CH2 CH3+NaCl+H2O,故答案为:3,4-二甲基-3-己烯;CH3CH2CH(CH3)-CCl(CH3)CH2 CH3+NaOH![]() CH3CH2C(CH3)=C(CH3)CH2 CH3+NaCl+H2O;
CH3CH2C(CH3)=C(CH3)CH2 CH3+NaCl+H2O;
(2)根据上述分析,A 生成B是消去反应,E在铁和氯化氢作用下发生还原反应生成F,C(CH3CH2COCH3)+F(![]() ) 生成G(
) 生成G(![]() )的化学方程式为CH3CH2COCH3+
)的化学方程式为CH3CH2COCH3+![]()
![]()
![]() + H2O,故答案为:消去反应;还原反应;CH3CH2COCH3+
+ H2O,故答案为:消去反应;还原反应;CH3CH2COCH3+![]()
![]()
![]() + H2O;CH3OH
+ H2O;CH3OH
(3)E(![]() )的同分异构体中,含有苯环和氨基且能与碳酸氢钠反应生成CO2的结构中含有苯环、氨基和羧基,①含有苯环、氨基和羧基和甲基的有10种;②含有苯环、氨基和—CH2COOH的有3种;③含有苯环、羧基和—CH2NH2的有3种;④含有苯环和—CH(NH2)COOH的1种,共17种;其中核磁共振氢谱有五组峰,峰面积之比为1:2:2:2:2的结构简式为
)的同分异构体中,含有苯环和氨基且能与碳酸氢钠反应生成CO2的结构中含有苯环、氨基和羧基,①含有苯环、氨基和羧基和甲基的有10种;②含有苯环、氨基和—CH2COOH的有3种;③含有苯环、羧基和—CH2NH2的有3种;④含有苯环和—CH(NH2)COOH的1种,共17种;其中核磁共振氢谱有五组峰,峰面积之比为1:2:2:2:2的结构简式为![]() 或
或![]() ,故答案为:17;
,故答案为:17;![]() 或
或![]() ;
;
(4)已知![]() ,以乙烯合成聚丙烯酸钠,要合成聚丙烯酸钠(
,以乙烯合成聚丙烯酸钠,要合成聚丙烯酸钠(![]() ),需要由乙烯增长碳链,根据已知信息,可以由乙烯先制备乙炔,乙炔与CO和醇反应生成
),需要由乙烯增长碳链,根据已知信息,可以由乙烯先制备乙炔,乙炔与CO和醇反应生成![]() ,
,![]() 在碱性条件下水解生成丙烯酸钠,最后加聚即可,合成路线为:CH2 = CH2
在碱性条件下水解生成丙烯酸钠,最后加聚即可,合成路线为:CH2 = CH2![]() CH2 Br CH2 Br
CH2 Br CH2 Br![]() CH≡CH
CH≡CH![]() CH2 = CHCOOCH3
CH2 = CHCOOCH3![]() CH2 = CHCOONa
CH2 = CHCOONa![]()
![]() ,故答案为:CH2 = CH2
,故答案为:CH2 = CH2![]() CH2 Br CH2 Br
CH2 Br CH2 Br![]() CH≡CH
CH≡CH![]() CH2 = CHCOOCH3
CH2 = CHCOOCH3![]() CH2 = CHCOONa
CH2 = CHCOONa![]()
![]() 。
。

 名校课堂系列答案
名校课堂系列答案