��Ŀ����
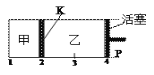
����Ŀ��ijѧϰС������ͼ��ʾA��Bװ�÷ֱ�̽������п��ϡ����ķ�Ӧ��ʵ�������Aװ���ձ��ڵ���Һ�¶����ߣ�Bװ�õĵ�����ָ�뷢��ƫת��

��1��Aװ�õ��ձ��з�����Ӧ�����ӷ���ʽΪ______________��
��2��Bװ����Zn����________����Cu���ϵ�������________���䷢���ĵ缫��Ӧʽ��_____ ������1 mol�����������ߣ����������ɵIJ�������ʵ���Ϊ_______ ��
��3��������ת���ĽǶȿ���A��B�з�Ӧ���������________��������������С�������������������������������A����Ҫ�ǽ���ѧ��ת��Ϊ__________��B����Ҫ�ǽ���ѧ��ת��Ϊ___________��
��4����С��ͬѧ��˼ԭ��ص�ԭ�������й۵���ȷ����___________������ĸ����
A ԭ��ط�Ӧ�Ĺ����п���û�е��ӷ���ת�� B ԭ���װ����Ҫ2���缫
C �缫һ�����ܲμӷ�Ӧ D ������Ӧ�ͻ�ԭ��Ӧ���Բ�����������
��5�������Ի�ѧ��Ӧ��2Zn��O2��4H��=2Zn2����2H2OΪ�������һ��ԭ��أ�������������Ϊ������������Դ�����ǿ�������ѪҺ������һ��Ũ�ȵ�O2��H����Zn2�����й��������ԭ��ص����������ĵ缫��ӦΪ___________��
���𰸡�Zn+2H+=Zn2++H2�� �� ������ð�� 2H++2e-=H2�� 0.5mol ���� ���� ���� BD O2 +4 H�� +4e-��2H2O
��������
(1)п�������ӷ�Ӧ����п������������
(2)пͭϡ����ԭ����У����ý���п��������пʧ���ӷ���������Ӧ��������������ͭ�ϵõ��ӷ�����ԭ��Ӧ��
(3)A�ձ����¶����ߣ��÷�Ӧ�Ƿ��ȷ�Ӧ��ԭ��ؽ���ѧ��ת���ɵ��ܣ�
(4)A��ԭ��صı������е���ת�ƣ�
B��ԭ��صĹ������������������缫��
C�����ý���������ʧ���ӷ���������Ӧ��
D����������������Ӧ������������ԭ��Ӧ��
(5)�ɷ�Ӧ2Zn+O2+4H+�T2Zn2++2H2O��֪��Zn����������Zn2+��������O2������ԭ��Ӧ������ΪH2O��
(1)п�������ӷ�Ӧ����п���������������ӷ���ʽΪZn+2H+�TZn2++H2����
(2)пͭϡ����ԭ����У����ý���п���������缫��ӦΪZn-2e-�TZn2+��������������ͭ�ϵõ��Ӳ����������缫��ӦΪ2H++2e-�TH2��������1 mol�����������ߣ����������ɵ�H2�����ʵ���Ϊ![]() =0.5mol��
=0.5mol��
(3)A�ձ����¶����ߣ��÷�Ӧ�Ƿ��ȷ�Ӧ�����Է�Ӧ���������������������������÷�Ӧ����ѧ��ת�������ܣ�ԭ����ǽ���ѧ��ת���ɵ��ܣ�
(4)A��ԭ���Ҫ���Է����е�������ԭ��Ӧ������һ���е��ӵ�ת�ƣ���A����
B��ԭ��صĹ������������������缫����B��ȷ��
C�����ý���������ʧ���ӷ���������Ӧ�������ϵõ��ӷ�����ԭ��Ӧ��һ�㸺���ܽ⣬�����������ػ��������壬��C����
D����������������Ӧ������������ԭ��Ӧ����D��ȷ��
�ʴ�Ϊ��BD��
(5)�ɷ�Ӧ2Zn+O2+4H+�T2Zn2++2H2O��֪��Zn����������Zn2+��������O2������ԭ��Ӧ������ΪH2O���缫��ӦʽΪO2 +4 H�� +4e-��2H2O��

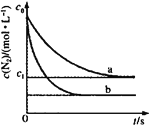
����Ŀ����һ���������з�Ӧ:2SO2(g)+O2(g)![]() 2SO3(g) ��H=-197kJ/mol.�����ݻ���ͬ�ļס��ҡ����������������������������·ֱ���������ͷ�Ӧ�ų�������(Q)�����ʾ:
2SO3(g) ��H=-197kJ/mol.�����ݻ���ͬ�ļס��ҡ����������������������������·ֱ���������ͷ�Ӧ�ų�������(Q)�����ʾ:
���� | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
�� | 2 | 1 | 0 | Q1 |
�� | 1 | 0.5 | 0 | Q2 |
�� | 1 | 0.5 | 1 | Q3 |
�����������ݣ�������������ȷ����:
A. Q1<197
B. �����������£���Ӧ����1molS03�������98.5kJ
C. Q2=Q3
D. Q3<Q1<2Q2
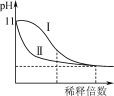
����Ŀ���̲��и�����Na2O2��ˮ��Ӧ�Ļ�ѧ����ʽ��ijѧϰС��ͨ��ʵ���о�Na2O2��ˮ����Ӧ����
���� | ���� |
�� | ���ҷ�Ӧ��������������ʹ������ľ����ȼ������ȫ���ܽ�õ�����ɫ��Һa |
�� | ��Һ��죬10���Ӻ���Һ��ɫ���Ա�dz���Ժ���Һ��Ϊ��ɫ |
�� | ���д������ݲ���������������Ҳ��ʹ������ľ����ȼ |
��1��Na2O2�ĵ���ʽΪ ______ �������ԣ�ʵ��֤ʵ����Һa��H2O2�Ĵ��ڣ�Ӧ��ͬλ��ʾ��ԭ�����Ա�ʾ��Ӧ�Ļ�����д��Na218O2��H2O��Ӧ�Ļ�ѧ����ʽ ______ ��
��2���������к�ɫ��ȥ�Ŀ���ԭ���� ______ ��
��3���÷�Ӧ![]() �ⶨ��Һa��H2O2������ȡ20.00ml��Һa����ϡ ______
�ⶨ��Һa��H2O2������ȡ20.00ml��Һa����ϡ ______ ![]() �ѧʽ
�ѧʽ![]() �ữ����0.002molL-1KMnO4��Һ�ζ������յ�ʱƽ������10.00ml KMnO4��Һ���ζ�ʱKMnO4��ҺӦװ�� ______
�ữ����0.002molL-1KMnO4��Һ�ζ������յ�ʱƽ������10.00ml KMnO4��Һ���ζ�ʱKMnO4��ҺӦװ�� ______ ![]() ������
������![]() ʽ�ζ����У��յ�ȷ���ķ����� ______ ����������Һa��c(H2O2)= ______ molL-1
ʽ�ζ����У��յ�ȷ���ķ����� ______ ����������Һa��c(H2O2)= ______ molL-1
��4������Һa�еμ�FeSO4��Һ��������Ӧ�����ӷ���ʽΪ______ ��
��5����FeSO4��Һ�м���һ����Na2O2���壬�������ʵ���Ϊ2��1������Ӧ����Ӧ�����������ɣ�д����Ӧ�����ӷ���ʽ ______ ��