题目内容
6.下列说法正确的是( )| A. | 苯在催化剂作用下能与溴水发生取代反应 | |
| B. | 实验室用CaC2和饱和食盐水制备乙炔 | |
| C. | 氯乙烷在氢氧化钠的水溶液中生成乙烯 | |
| D. | 将苯、浓HNO3的混合物用水浴加热(60℃左右)制备硝基苯 |
分析 A.苯与卤素发生取代反应的条件;
B.根据实验室制取乙炔反应原理分析;
C.根据卤代烃制取烯烃的条件分析;
D.根据硝基苯的制取条件判断.
解答 解:A.苯在催化剂作用下能与液溴发生取代反应,与溴水不反应,故A错误;
B.实验室用CaC2和饱和食盐水制备乙炔,故B正确;
C.氯乙烷在氢氧化钠的醇溶液中生成乙烯,而在水溶液中生成乙醇,故C错误;
D.将苯、浓HNO3的混合物用水浴加热(60℃左右)不能制备硝基苯,因缺少催化剂浓硫酸,故D错误,
故选B.
点评 本题考查了有机物的性质,有机反应是在一定条件下进行的,条件不同,反应类型不同,产物不同,要重视反应条件,书写方程式不漏掉反应条件.

练习册系列答案
相关题目
1.2012年4月22日是第43个“世界地球日”,其主题为“绿色梦 想,低碳行动”.下列做法符合这一主题的是( )
①开发太阳能、风能和氢能等能源
②大量开采地下水,以满足生产、生活的需求
③使用布袋购物、以步代车等属于“低碳生活”方式
④开发利用可燃冰是缓解能源紧缺的唯一途径
⑤利用可降解的“玉米塑料”生产一次性饭盒.
①开发太阳能、风能和氢能等能源
②大量开采地下水,以满足生产、生活的需求
③使用布袋购物、以步代车等属于“低碳生活”方式
④开发利用可燃冰是缓解能源紧缺的唯一途径
⑤利用可降解的“玉米塑料”生产一次性饭盒.
| A. | ①③⑤ | B. | ①②③ | C. | ②④⑤ | D. | ①②④ |
11.下列化学用语表示正确的是( )
| A. | Cl-的结构示意图: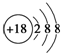 | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | 氢氧化钠的电子式: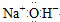 | D. | 铁元素不属于主族元素 |
15.下列各组离子能在指定溶液中大量共存的一组是( )
| A. | 在稀盐酸中:Ba2+、CO32-、Zn2+ | B. | 在氢氧化钠溶液中:H+、Mg2+、Cl- | ||
| C. | 在硫酸铵溶液中:Na+、K+、OH- | D. | 在氯化钠溶液中:K+、Ca2+、N03- |
16.下列说法错误的是( )
| A. | 金属元素在不同化合物中化合价均不同 | |
| B. | 钾的金属性强,所以钾与水的反应比钠的反应剧烈 | |
| C. | 食物放在冰箱中会减慢食物变质的速率 | |
| D. | 面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸 |
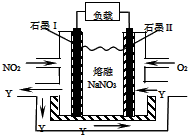 (1)为了证明一水合氨是弱碱,甲、乙、丙三同学分别设计以下实验进行探究.
(1)为了证明一水合氨是弱碱,甲、乙、丙三同学分别设计以下实验进行探究.
 、
、 、
、 ;
;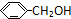 ;
;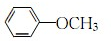 .
.