题目内容
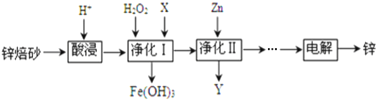
【题目】工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质)制取金属锌的工艺流程如下:
回答下列问题:
(1)ZnFe2O4是一种性能优良的软磁材料,也是一种催化剂,能催化烯类有机物氧化脱氢等反应。
① ZnFe2O4中Fe的化合价是___________,从物质分类角度说,ZnFe2O4属于__________(填“酸”、“碱”或“盐”)。
② 工业上利用反应ZnFe2(C2O4)3·6H2O![]() ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是______________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。
ZnFe2O4+2CO2↑+4CO↑+6H2O制备ZnFe2O4。该反应中氧化产物是______________(填化学式),每生成1mol ZnFe2O4,转移电子的物质的量是___________。
(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率。为达到这一目的,还可采用的措施是___________(任答一条);已知ZnFe2O4能溶于酸,则酸浸后溶液中存在的金属离子有______________。
(3)净化Ⅰ中H2O2参与反应的离子方程式为_______________;试剂X的作用是___________。
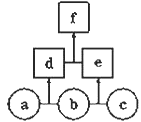
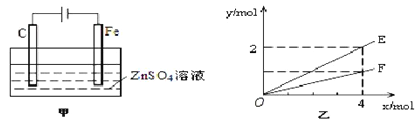
(4)钢铁镀锌是钢铁防护的一种有效方法。按图甲装置进行模拟铁上镀锌的实验,实验结果如图乙所示。乙中横坐标x表示电路中通过电子的物质的量,纵坐标y表示反应物或生成物的物质的量。
① C电极的电极反应式为________________________。
② E可以表示的量是_________________________(任写一种)。
【答案】
(1)①+3;盐;②ZnFe2O4、CO2;4mol;
(2)增大硫酸的浓度(或升高温度、空气搅拌等);Zn2+、Fe3+、Fe2+、Cu2+;
(3)H2O2+2Fe2++2H+=2Fe3++2H2O;调节溶液的pH,促进Fe3+水解;
(4)①4OH--4e-=O2+2H2O;②消耗水的物质的量、生成硫酸的物质的量、生成Zn的物质的量等任写一种。
【解析】
试题分析:(1) ① 根据正负化合价的代数和为0,ZnFe2O4中Fe的化合价是+3,从物质分类角度说,ZnFe2O4属于盐,故答案为:+3;盐;
② 在反应ZnFe2(C2O4)3·6H2O![]() ZnFe2O4+2CO2↑+4CO↑+6H2O中铁元素的化合价由+2价升高到+3价,被氧化,碳元素的化合价由+3价变成+2价和+4价,氧化产物为ZnFe2O4和CO2,每生成1mol ZnFe2O4同时生成2mol二氧化碳,转移电子的物质的量为1mol ×(3-2)×2+2mol×(2-1)=4mol,故答案为:ZnFe2O4、CO2;4mol;
ZnFe2O4+2CO2↑+4CO↑+6H2O中铁元素的化合价由+2价升高到+3价,被氧化,碳元素的化合价由+3价变成+2价和+4价,氧化产物为ZnFe2O4和CO2,每生成1mol ZnFe2O4同时生成2mol二氧化碳,转移电子的物质的量为1mol ×(3-2)×2+2mol×(2-1)=4mol,故答案为:ZnFe2O4、CO2;4mol;
(2)酸浸时要将锌焙砂粉碎,其目的是提高酸浸效率,还可采用的措施有增大硫酸的浓度、升高温度、空气搅拌等;锌焙砂主要含ZnO、ZnFe2O4,还含有少量FeO、CuO等杂质,其中ZnFe2O4能溶于酸,ZnO、FeO、CuO也都能溶于酸,酸浸后溶液中存在的金属离子有Zn2+、Fe3+、Fe2+、Cu2+,故答案为:增大硫酸的浓度(或升高温度、空气搅拌等);Zn2+、Fe3+、Fe2+、Cu2+;
(3)净化Ⅰ中H2O2将亚铁离子氧化,反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O;试剂X可以调节溶液的pH,促进Fe3+水解,故答案为H2O2+2Fe2++2H+=2Fe3++2H2O;调节溶液的pH,促进Fe3+水解;
(4)由甲可知,为电解装置,C为阳极,发生4OH--4e-=O2↑+2H2O,铁为阴极,发生Zn2++2e-=Zn,总反应为2ZnSO4+2H2O![]() 2Zn+O2↑+2H2SO4,结合乙可知,转移4mol电子生成2molE,生成1molF,由电子与物质的物质的量的关系可知E表示反应生成铜的物质的量,由总反应可知,Cu与水的物质的量相同,则E表示反应消耗水的物质的量或生成硫酸的物质的量等,故答案为:①4OH--4e-=O2+2H2O;②消耗水的物质的量(或生成硫酸的物质的量、或生成Zn的物质的量)。
2Zn+O2↑+2H2SO4,结合乙可知,转移4mol电子生成2molE,生成1molF,由电子与物质的物质的量的关系可知E表示反应生成铜的物质的量,由总反应可知,Cu与水的物质的量相同,则E表示反应消耗水的物质的量或生成硫酸的物质的量等,故答案为:①4OH--4e-=O2+2H2O;②消耗水的物质的量(或生成硫酸的物质的量、或生成Zn的物质的量)。

 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案【题目】
成分的质量/g | 摩尔质量/(gmol-1) | |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.02 | 170 |
(1)下列“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为__________molL-1(要求:用原始数据写出表达式即可,不需要化简与计算)。
(2)配制上述“鲜花保鲜剂”所需的仪器有烧杯、玻璃棒、药匙、托盘天平(带砝码)、
____________________(填所缺仪器的名称)。
(3)在溶液配制过程中,下列操作对配制结果没有影响的是_________(填字母).
A.定容时,俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)若要配制0.5mol·L-1500ml的硫酸溶液,则:
①所需质量分数为98%、密度为1.84g·cm-3的浓硫酸的体积为___________(计算结果保留一位小数)mL;
②如果实验室有15mL、20mL、50mL量筒,应选用___________mL量筒最好;
③配制过程中需先在烧杯中将浓硫酸稀释,稀释时操作方法是_____________________.