题目内容
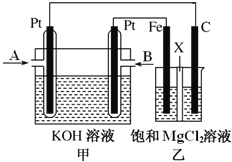
【题目】下图中甲为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,乙为电解饱和MgCl2溶液的装置,其中乙装置中X为阳离子交换膜。用该装置进行实验,反应开始后观察到Fe电极附近出现白色沉淀。下列说法正确的是
A. 甲中A处通入CH4,电极反应式为CH4+10OH--8e-=== ![]() +7H2O
+7H2O
B. 乙中电解MgCl2溶液的总反应为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. 理论上甲中每消耗22.4 L CH4(标准状况下),乙中产生4 mol Cl2
D. 甲、乙中电解质溶液的pH都增大
【答案】C
【解析】A项,乙为电解氯化镁溶液的装置,反应开始后观察到Fe电极附近出现白色沉淀,说明H+在铁电极放电,所以铁电极为阴极,则甲中B端为负极,通入CH4,反生氧化反应,电极反应式为:CH4+10OH--8e-=CO32-+7H2O,故A错误;B项,乙中电解氯化镁溶液的总反应为:Mg2++2Cl-+2H2O![]() Cl2↑+H2↑+Mg(OH)2↓,故B错误;C项,由上分析可知,甲中每消耗标况下22.4L(1mol)CH4,转移8mol电子,则乙中产生4molCl2,故C正确;D项,甲中KOH参与反应,碱性减弱,PH减小,乙中氢离子放电,pH增大,故D错误。
Cl2↑+H2↑+Mg(OH)2↓,故B错误;C项,由上分析可知,甲中每消耗标况下22.4L(1mol)CH4,转移8mol电子,则乙中产生4molCl2,故C正确;D项,甲中KOH参与反应,碱性减弱,PH减小,乙中氢离子放电,pH增大,故D错误。

练习册系列答案
相关题目
【题目】对下列实验现象的解释不正确的是
选项 | 实验现象 | 解释 |
A | C12使鲜艳的红色花瓣褪色 | Cl2具有强还原性 |
B | NH3与HCl气体接触时有白烟产生 | NH3与HCl反应生成固体小颗粒 |
C | 新切开的Na表面在空气中很快变暗 | Na容易与空气中的氧气等反应 |
D | 氯化铝溶液中滴入过量的氢氧化钠溶液,白色沉淀溶解 | 氢氧化铝具有两性 |
A. A B. B C. C D. D