题目内容
17.T℃时在2L的密闭容器中X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图(1)所示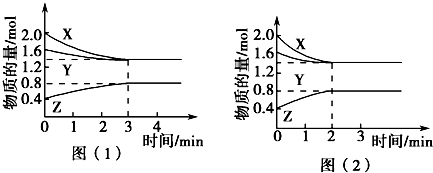
(1)容器中发生的可逆反应的反应方程式为3X+Y═2Z;
(2)反应进行的前3min内,用X表示的反应速率v(X)=0.1mol•(L•min)-1;
(3)该可逆反应T℃时的化学平衡常数K≈0.67(保留小数点后两位);
若在3min到达平衡后的某一时刻再分别加入0.6mol Y及0.4molZ(维持体积、温度不变),则平衡将往逆向移动;
(4)若维持T℃温度不变且保持压强不变,在体积可变的弹性容器中起始时只充入a mol X和 b mol Y,若要保证达到平衡时与图(1)中X、Y、Z各物质体积分数相同,则a、b需满足$\frac{a}{b}$=$\frac{13}{9}$;
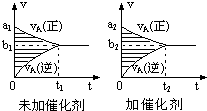
(5)若改变反应条件,使反应进程如图(2)所示,则改变的条件是加入催化剂.
分析 (1)根据图知,随着反应进行,X、Y的物质的量减小而生成物物质的量增大,则X、Y是反应物而Z是生成物,反应达到平衡状态时,△n(X)=(2.0-1.4)mol=0.6mol,△n(Y)=(1.6-1.4)mol=0.2mol,△n(Z)=(0.8-0.4)mol=0.4mol,同一化学反应中同一时间段内各物质的物质的量之比等于其计量数之比,据此确定化学式;
(2)用X表示的反应速率v(X)=$\frac{\frac{0.6mol}{2L}}{3min}$;
(3)化学平衡时,c(X)=$\frac{1.4mol}{2L}$=0.7mol/L、c(Y)=$\frac{1.4mol}{2L}$=0.7mol/L、c(Z)=$\frac{0.8mol}{2L}$=0.4mol/L,化学平衡常数K=$\frac{0.4×0.4}{0.{7}^{3}×0.7}$;
加入Y、Z后容器中c(X)=0.7mol/L、c(Y)=$\frac{1.4+0.6}{2}$mol/L=1mol/L、c(Z)=$\frac{0.8+0.4}{2}$mol/L=0.6mol/L,浓度商=$\frac{0.6×0.6}{0.{7}^{3}×1}$,根据浓度商与化学平衡常数K之间的相对大小判断平衡移动方向;
(4)反应达到平衡状态时,与图(1)中X、Y、Z各物质体积分数相同,设参加反应的Y的物质的量为xmol,
3X+Y═2Z
amol bmol 0
3xmolxmol 2xmol
(a-3x)mol (b-x)mol 2x
图(1)平衡时X、Y的物质的量相等,所以其体积分数相等,则(a-3x)mol=(b-x)mol,x=$\frac{a-b}{2}$,
图(1)中平衡时Z的体积分数=$\frac{0.8mol}{(1.4+1.4+0.8)mol}$=$\frac{2}{9}$,
则$\frac{2x}{(a-3x)+(b-x)+2x}$=$\frac{2}{9}$,据此计算a、b关系式;
(5)根据图2知,反应达到平衡状态时,各物质的物质的量与图(1)相同,但反应时间缩短,说明改变条件时增大反应速率但不影响平衡移动.
解答 解:(1)根据图知,随着反应进行,X、Y的物质的量减小而生成物物质的量增大,则X、Y是反应物而Z是生成物,反应达到平衡状态时,△n(X)=(2.0-1.4)mol=0.6mol,△n(Y)=(1.6-1.4)mol=0.2mol,△n(Z)=(0.8-0.4)mol=0.4mol,同一化学反应中同一时间段内各物质的物质的量之比等于其计量数之比,则X、Y、Z的计量数之比为0.6mol:0.2mol:0.4mol=3:1:2,则该反应方程式为3X+Y═2Z,
故答案为:3X+Y═2Z;
(2)用X表示的反应速率v(X)=$\frac{\frac{0.6mol}{2L}}{3min}$=0.1mol•(L•min)-1,故答案为:0.1;
(33)化学平衡时,c(X)=$\frac{1.4mol}{2L}$=0.7mol/L、c(Y)=$\frac{1.4mol}{2L}$=0.7mol/L、c(Z)=$\frac{0.8mol}{2L}$=0.4mol/L,化学平衡常数K=$\frac{0.4×0.4}{0.{7}^{3}×0.7}$≈0.67;
加入Y、Z后容器中c(X)=0.7mol/L、c(Y)=$\frac{1.4+0.6}{2}$mol/L=1mol/L、c(Z)=$\frac{0.8+0.4}{2}$mol/L=0.6mol/L,浓度商=$\frac{0.6×0.6}{0.{7}^{3}×1}$=1.05>0.67,则该反应向逆反应方向移动;
故答案为:0.67;逆向;
(4)反应达到平衡状态时,与图(1)中X、Y、Z各物质体积分数相同,设参加反应的Y的物质的量为xmol,
3X+Y═2Z
amol bmol 0
3xmolxmol 2xmol
(a-3x)mol (b-x)mol 2x
图(1)平衡时X、Y的物质的量相等,所以其体积分数相等,则(a-3x)mol=(b-x)mol,x=$\frac{a-b}{2}$,
图(1)中平衡时Z的体积分数=$\frac{0.8mol}{(1.4+1.4+0.8)mol}$=$\frac{2}{9}$,
则$\frac{2x}{(a-3x)+(b-x)+2x}$=$\frac{2}{9}$,a、b关系式为$\frac{a}{b}$=$\frac{13}{9}$,
故答案为:$\frac{a}{b}$=$\frac{13}{9}$;
(5)根据图2知,反应达到平衡状态时,各物质的物质的量与图(1)相同,但反应时间缩短,说明改变条件时增大反应速率但不影响平衡移动,催化剂能同等程度的改变正逆反应速率但不影响平衡移动,所以改变的体积是加入催化剂,故答案为:催化剂.
点评 本题考查化学平衡有关计算、化学平衡影响因素等知识点,为高频考点,侧重考查学生分析计算能力,难点是等效平衡的有关计算,要充分利用体积分数相等进行计算,注意催化剂只改变反应速率但不影响平衡移动,为易错点.

| A. | 分子数 | B. | 颜色 | C. | 原子数 | D. | 密度 |
| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| A. | 该反应的正方应为吸热反应 | |
| B. | 若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行 | |
| C. | 容器I中反应达到平衡所需时间比容器Ⅲ中的长 | |
| D. | 达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小 |
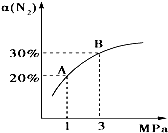 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A. | 将1.0 mol氮气、3.0 mol氢气,置于1 L密闭容器中发生反应,放出的热量为 92.4 kJ | |
| B. | 平衡状态由A变到B时,平衡常数K (A)<K (B) | |
| C. | 上述反应在达到平衡后,增大压强,H2的转化率提高 | |
| D. | 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速度减小 |
| A. | 加入稀H2SO4,过滤 | B. | 加入NaCl溶液,过滤 | ||
| C. | 加入NaOH溶液,过滤 | D. | 加入CuSO4溶液,过滤 |
| 元素 | 有 关 信 息 |
| A | 元素主要化合价为-2,原子半径为0.074nm |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子半径为0.102nm,其单质为黄色晶体,可在A的单质中燃烧 |
| D | 最高价氧化物的水化物能按1:1电离出电子数相等的阴、阳离子 |
| E | 原子半径为0.075nm,最高价氧化物的水化物可与其氢化物形成一种盐X |
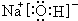 ;
;(2)写出B单质与水反应的离子方程式Cl2+H2O=Cl-+H++HClO;
(3)元素A和D形成的某种化合物可作为呼吸面具中氧气的来源,写出得到氧气反应的主要化学方程式2Na2O2+2CO2═2Na2CO3+O2;
(4)已知E元素的某种氢化物Y与A2的摩尔质量相同,Y与空气组成的燃料电池中,电解质溶液是30%的KOH溶液,该电池放电时正极的电极反应式为O2+2H2O+4e-═4OH-;
(5)若使用Y-空气燃料电池精炼铜,当得到精铜80g时,燃料电池中转移的电子数为2.5NA.
 )
)