题目内容
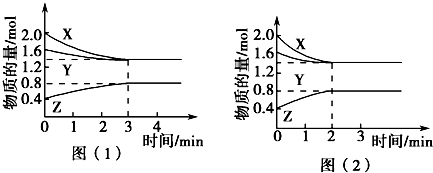
5.一定温度下,在三个体积约为1.0L的恒容密闭容器中发生反应:2CH3OH(g)?CH3OCH3(g)+H2O(g)| 容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
| I | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 387 | 0.40 | ||
| Ⅲ | 207 | 0.20 | 0.090 | 0.090 |
| A. | 该反应的正方应为吸热反应 | |
| B. | 若起始时向容器I中充入CH3OH 0.1mol、CH3OCH3 0.15mol和H2O 0.10mol,则反应将向正反应方向进行 | |
| C. | 容器I中反应达到平衡所需时间比容器Ⅲ中的长 | |
| D. | 达到平衡时,容器I中的CH3OH体积分数比容器Ⅱ中的小 |
分析 A.根据温度与化学平衡常数的关系确定反应热;
B.根据化学平衡常数与浓度商的相对大小判断反应方向,如果浓度商小于平衡常数,则平衡向正反应方向进行;
C.温度越高,反应速率越大,反应时间越短;
D.该反应是反应前后气体体积不变的反应,温度相同,化学平衡常数相同,反应物的转化率相同.
解答 解:A.容器Ⅰ中平衡时c(CH3OCH3)=c(H2O)=$\frac{0.080mol}{1.0L}$=0.080mol/L,c(CH3OH)=$\frac{0.2mol-0.080mol×2}{1.0L}$=0.04mol/L,容器Ⅰ中化学平衡常数K1=$\frac{0.08×0.08}{0.04×0.04}$=4,容器Ⅲ中平衡时c(CH3OCH3)=c(H2O)=$\frac{0.090mol}{1.0L}$=0.090mol/L,c(CH3OH)=$\frac{0.2mol-0.00mol×2}{1.0L}$=0.02mol/L,化学平衡常数K2=$\frac{0.09×0.09}{0.02×0.02}$=20.25>4,所以降低温度,化学平衡常数增大,反应向正反应方向移动,则正反应是放热反应,故A错误;
B.c(CH3OH)=0.1mol/L、c(CH3OCH3 )=0.15mol/L、c(H2O)=0.10mol/L,浓度商=$\frac{0.1×0.15}{0.1×0.1}$=1.5<4,平衡向正反应方向移动,故B正确;
C.容器I中的温度比容器III的温度高,温度越高反应速率越快,达到平衡所需时间越短,故C错误;
D.恒容条件下,容器Ⅱ相当于在容器Ⅰ的基础上加压,但由于该反应是反应前后气体体积不变的反应,因此平衡不移动,所以容器Ⅰ中的CH3OH体积分数和容器Ⅱ中的相等,故D错误;
故选B.
点评 本题考查了化学平衡常数的有关计算,根据平衡常数公式计算平衡常数,再结合浓度与反应速率的关系、化学平衡常数与浓度商之间的关系来分析解答,注意该反应特点,题目难度中等.

| A. | 铁粉与盐酸反应:2Fe+6H+═3H2↑+2 Fe3+ | |
| B. | 将铜片投入硫酸溶液中:Cu+2H+═H2↑+Cu2+ | |
| C. | 硫酸溶液与氢氧化钡溶液反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 向澄清石灰水中滴入少量碳酸氢钠溶液:HCO${\;}_{3}^{-}$+OH-+Ca2+═CaCO3↓+H2O |
| A. | v(A)=3.6 mol•L-1•s-1 | B. | v(B)=0.075 mol•L-1•s-1 | ||
| C. | v(C)=0.030 mol•L-1•s-1 | D. | v(D)=0.060 mol•L-1•s-1 |
| A. | 单位物质的量的气体所占的体积就是气体摩尔体积 | |
| B. | 通常状况(室温、101kP)下,气体摩尔体积约为22.4 L/mol | |
| C. | 标准状况(0℃、101kP)下,气体摩尔体积约为22.4 L/mol | |
| D. | 标准状况(0℃、101kP)下,1 mol H2O的体积是22.4 L |
| A. | 甲烷的燃烧热△H=-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 一定条件下,将0.5 mol N2和1.5 molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| C. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | |
| D. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| A. | 2NO2(g)(红棕色)???N2O4(g)(无色)△H<0,在平衡后,对平衡体系采取缩小容积、增大压强的措施,因为平衡向正反应方向移动,故体系颜色变浅 | |
| B. | H2(g)+I2(g)???2HI(g)△H<0,在平衡后,对平衡体系采取增大容积、减小压强的措施,因为平衡不移动,故体系颜色不变 | |
| C. | FeCl3+3KSCN???Fe(SCN)3(红色)+3KCl,在平衡后,加少量KCl,因为平衡向逆反应方向移动,故体系颜色变浅 | |
| D. | 对于N2+3H2???2NH3,平衡后,压强不变,充入O2,平衡左移 |
| A. | 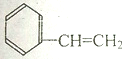 | B. | 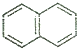 | C. |  | D. | 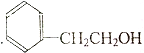 |
| 周期 族 | IA | 0 | ||||||
| 1 | ① | IIA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ | ||||||
(2)这些元素的最高价氧化物对应水化物中酸性最强的是HClO4,碱性最强的是KOH(填化学式)
(3)气态氢化物能与其最高价氧化物对应的水化物反应生成盐的化学方程式为:NH3+HNO3=NH4NO3.
(4)呈两性的氢氧化物分别与④和⑥的最高价氧化物对应的水化物反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,Al(OH)3+3H+=Al3++3H2O.