题目内容
【题目】N、P同属于元素周期表的第VA族元素。
(1)基态磷原子的价电子排布图是____________
(2)NCl3的VSEPR模型名称是,中心原子杂化轨道类型是__________________。
(3)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为原子总数相同、价电子总数相同的粒子即等电子体具有相似的化学键特征,它们的许多性质是接近的。写出N2O的一种有第二周期非金属元素组成的等电子体分子。
(4)沸点比较:PH3NH3(填“>”、“=”、“<”),理由是____________。
(5)已知键能:H-H键能为436KJ·mol-1,N-H键能为391KJ·mol-1,N≡N键能为945.6kJmol-1.。则N2+3H2![]() 2NH3,生成2molNH3时,共放热_________KJ
2NH3,生成2molNH3时,共放热_________KJ
(6)NH3极易溶于水,原因是_______________
【答案】(1)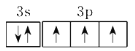
(2)四面形,sp3杂化轨道
(3)CO2
(4)<NH3分子之间有氢键
(5)92.4(2分)
(6)NH3和水都是极性分子,相似相溶;NH3和水分子之间有氢键;NH3和水要发生化学反应(3分)
【解析】
试题分析:
(1)基态磷原子的价电子排布式为3s23p3,根据泡利原理和洪特规则可得价电子排布图为 。
。
(2)根据价层电子对互斥理论,NCl3中氮原子含有的孤对电子对数是(5-1×3)÷2=1,N原子的价层电子对数为3+1=4,则NCl3的VSEPR模型名称是四面体,中心原子杂化轨道属于sp3杂化。
(3)根据等电子体的特点,原子总数相同、价电子总数相同的即为等电子体。N2O的原子个数为3个,价电子数为16。则由第二周期非金属元素组成的等电子体分子为CO2。
(4)因NH3分子之间有氢键,沸点比PH3高。
(5)H-H键能为436KJ·mol-1,N-H键能为391KJ·mol-1,N≡N键能为945.6kJmol-1.。对于反应N2+3H2![]() 2NH3的反应热=反应物的总键能-生成物的总键能=945.6kJmol-1+436KJ·mol-1×3-391KJ·mol-1×6=-92.4KJ·mol-1,则生成2molNH3时,共放热92.4KJ。
2NH3的反应热=反应物的总键能-生成物的总键能=945.6kJmol-1+436KJ·mol-1×3-391KJ·mol-1×6=-92.4KJ·mol-1,则生成2molNH3时,共放热92.4KJ。
(6)NH3极易溶于水,是因为NH3和水都是极性分子,相似相溶;NH3和水分子之间有氢键;NH3和水要发生化学反应。

 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案