题目内容
已知可逆反应CO+H2O(g)  CO2+H2,达到平衡时,K=
CO2+H2,达到平衡时,K=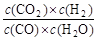 ,K是常数,只与温度有关,与浓度无关。
,K是常数,只与温度有关,与浓度无关。
(1)830K时,若起始时:c(CO)=2mol/L,c(H2O)=3mol/L,平衡时CO的转化率为60%,水蒸气的转化率为 ;K值为 。
(2)830K,若只将起始时c(H2O)改为6mol/L,则水蒸气的转化率为 。
(3)若830K时,起始浓度c(CO)=a mol/L,c(H2O)=b mol/L,H2的平衡浓度c(H2)=c mol/L,a、b、c之间的关系式是 。
【答案】
(1)40%,1(2)25%(3)C2=(a-c)(b-c)
【解析】
试题分析:(1)平衡时CO的转化率为60%,则转化的浓度为1.2 mol/L,平衡时CO的浓度为0.8 mol/L ,;水蒸气的转化浓度为1.2
mol/L,转化率为1.2mol÷3mol/L×100%=40%;平衡时CO2和H2的浓度均为0.8 mol/L,故K值为1;(2)设此时各物质的转化浓度均为xmol/L,则平衡时,CO的浓度为(2-x)mol/L,水蒸气的浓度为(6-x)mol/L,二氧化碳和氢气的浓度均为xmol/L;因为K只与温度有关,故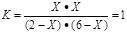 ,解得X=1.5,故水蒸气的转化率为1.5mol/L÷6mol/L×100%=25%;(3)因H2的平衡浓度c(H2)=c mol/L,故四种物质的转化浓度均为c
mol/L,平衡时,CO的浓度为(a-c)mol/L,水蒸气的浓度为(b-c)mol/L,故
,解得X=1.5,故水蒸气的转化率为1.5mol/L÷6mol/L×100%=25%;(3)因H2的平衡浓度c(H2)=c mol/L,故四种物质的转化浓度均为c
mol/L,平衡时,CO的浓度为(a-c)mol/L,水蒸气的浓度为(b-c)mol/L,故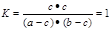 ,即C2=(a-c)(b-c)。
,即C2=(a-c)(b-c)。
考点:化学平衡
点评:化学平衡是历年高考重中之重,考生一定要系统备考此知识点。难度较大。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 CO2(g)+H2(g) ΔH<0,反应达到平衡状态后,欲提高CO的转化率,可以采取的措施为
CO2(g)+H2(g) ΔH<0,反应达到平衡状态后,欲提高CO的转化率,可以采取的措施为