��Ŀ����
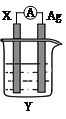
����Ŀ������������ԭ��Ӧ��2Ag��(aq)��Cu(s)��Cu2��(aq)��2Ag(s)��Ƶ�ԭ�����ͼ��ʾ��
��ش��������⣺
��1�� �缫X�IJ�����______���������ҺY��________��
��2�� ���缫Ϊ��ص�__________���������ĵ缫��ӦʽΪ____________��X�缫�Ϸ����ĵ缫��ӦΪ______��Ӧ��������������������ԭ����
��3�� ���·�еĵ���_________������������������������Ag�缫��
��4�� ����1.6 gͭ�ܽ�ʱ����������______ g��
���𰸡�Cu AgNO3 �� Ag++e��=Ag ������Ӧ ���� 5.4
��������
��1�������ܷ�Ӧ����ʽ��Cu�Ļ��ϼ����ߣ�Ag�����ϼ۽��ͣ�����ԭ��صĹ���������XΪCu��YΪAgNO3��
(2)�����������������������������ĵ缫��ӦʽΪ��Ag����e��=Ag��X�缫�ϵķ�ӦʽΪCu��2e��=Cu2�������ϼ����ߣ�������������������Ӧ��
��3������ԭ��صĹ���ԭ�������ӴӸ��������·��������������ͭ�����·��ͭ��
��4��������Cu��2e��=Cu2����������Ag����e��=Ag�����ݵ�ʧ������Ŀ�غ㣬n(Cu)=1.6/64mol=0.025mol��ʧȥ���ӵ����ʵ���Ϊ0.025��2mol=0.05mol���������m(Ag)=108��0.05g=5.4g��

 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�����Ŀ�������仯������NH3����Ρ�N2H4��N2O4������ѧ��ѧ��������ҵ������������ռ����Ҫ��λ��
(1)���亽����������(N2H4)��N2O4��ȼ������ȼ������(N2H4)��N2O4�ķ�ӦΪ
2N2H4 (g)+ N2O4(g)==3N2(g)+4H2O(g) ��H=-1077 kJ��mol-1��
��֪��ط�Ӧ�Ļ�ѧ�������������±���ʾ��
��ѧ�� | N��H | N��N |
| O��H |
E/(kJ��mol��1) | 390 | 190 | 946 | 460 |
��ʹ1 mol N2O4(g)�����л�ѧ����ȫ����ʱ��Ҫ���յ�������________________��
��������˵��2N2H4 (g)+ N2O4(g)==3N2(g)+4H2O(g) ��H ��ƽ��״̬����________
a.��������ƽ����Է����������� b.V��N2��=3V�� N2O4��
c.N2H4���������ֲ��� d. ��H���ٱ仯
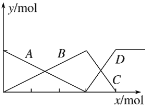
(2)N2O4��NO2֮����ڷ�ӦN2O4(g) ![]() 2NO2(g)����һ������N2O4���˺����ܱ������У������ƽ��ת����[��(N2O4)]���¶ȵı仯����ͼ��ʾ��
2NO2(g)����һ������N2O4���˺����ܱ������У������ƽ��ת����[��(N2O4)]���¶ȵı仯����ͼ��ʾ��

����ͼ�Ʋ�÷�Ӧ�ġ�H_______0(��>����<��)������Ϊ____________________________��
��ͼ��a���Ӧ�¶��£���֪N2O4����ʼѹǿp0Ϊ108 kPa������¶��·�Ӧ��ƽ�ⳣ��Kp��________________ (��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
(3)���NO2�Ʊ�NH4NO3���乤��ԭ������ͼ��ʾ��

�������ĵ缫��ӦʽΪ____________________________________________________��
��Ϊʹ������ȫ��ת��ΪNH4NO3���貹��ij�ֻ����������A����A�Ļ�ѧʽΪ________________��
����Ŀ����Ԫ�ؿ��γɶ��ֻ�����ڹ�ҵ�����о�����Ҫ��ֵ����ش��������⣺
(1)һ���¶��£���һ������N2��H2����̶�������ܱ������н��кϳɰ���Ӧ��
������������˵���ÿ��淴Ӧ�ﵽ��ѧƽ��״̬����__��
A.������������ܶȲ���
B.c(N2)��c(H2)��c(NH3)=1��3��2
C.�����ڵ�ѹǿ����
D.��ͬʱ������3molH-H�����ѣ���6molN-H���γ�
E.3v��(H2)=2v��(NH3)
F.�����������ƽ����Է�����������
�ں��º�ѹ�����£�Ϊ��ߺϳɰ���Ӧ��N2��H2�������ʣ��ɲ��õķ���__(һ�ּ���)��
(2)һ���¶��£�2L�ܱ������г���0.40molN2O4��������Ӧ��N2O4(g)![]() 2NO2(g)��һ��ʱ���ﵽƽ�⣬����������£�
2NO2(g)��һ��ʱ���ﵽƽ�⣬����������£�
ʱ��/s | 20 | 40 | 60 | 80 | 100 |
c(NO2)/(mol/L) | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
��20s�ڣ�v(NO2)=__�����¶��·�Ӧ�Ļ�ѧƽ�ⳣ����ֵΪ__��
�������¶�ʱ��������ɫ���������Ӧ��__(��������������������)��Ӧ��
����ͬ�¶��£�����ʼ��������г���0.40mo1NO2����ﵽƽ���c(NO2)__0.15mol/L(����>������=������<��)