题目内容
在标准状况下,将44.8LHCl溶于927mL水(密度为1g/cm3)中,所得盐酸的密度为1.05g/cm3,计算所得盐酸的溶质质量分数及物质的量浓度。
7.3% 2.1mol/L
解析试题分析:标准状况下,44.8LHCl物质的量为n(HCl)=44.8L÷22.4L/mol=2mol,质量为m(HCl)=2mol×36.5g/mol=73g,927ml水的质量为927g,则溶液的质量为:927g+73g=1000g,所以盐酸的质量分数为:73g÷1000g÷×100%=7.3%;所得盐酸的物质的量浓度为:c(HCl)=2mol÷(1000g÷1050g/L)=2.1mol?L?1。
考点:本题考查溶质质量分数、物质的量浓度的计算

练习册系列答案
相关题目
等质量的两种金属粉末A、B分别与同浓度的足量稀盐酸反应,都生成+2价金属氯化物,其反应情况如图所示: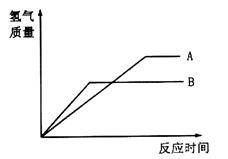
(1)在Fe、Zn、Cu中,A是__________,B是____________。
(2)将两种金属粉末按一定比例混合后,进行甲、乙、丙三组实验,三组实验各取500mL同浓度的盐酸加入该种混合粉末,有关数据如下:
| 实验序号 | 甲 | 乙 | 丙 |
| 混合粉末质量/g | 6.2 | 18.6 | 24.8 |
| 生成气体体积(标准状况下)/mL | 2240 | 5600 | 5600 |
计算上述所用盐酸的物质的量浓度(写出计算过程)中。


 的物质的量浓度;
的物质的量浓度;