题目内容
奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是食品与硫酸和催化剂一同加热,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
操作步骤:
①样品处理:准确称取一定量的固体样品奶粉,移入干燥的烧杯中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
②NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸铵,再经过碱化蒸馏后,氨即成为游离态,游离氨经硼酸吸收。
③氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,由消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
试回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水?
________________________________________________________________________________________________________________________________________________。
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大( )
| A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯 |
| B.定容时,俯视刻度线 |
| C.定容时,仰视刻度线 |
| D.移液时,有少量液体溅出 |
[已知:滴定过程中涉及到的反应方程式:(NH4)2B4O7+2HCl+5H2O===2NH4Cl+4H3BO3]
(1)往容量瓶中注入一定量的水,塞紧瓶塞,倒转过来,观察是否漏水,然后再正放,旋转瓶塞180°,再倒转过来,观察是否漏水,若都不漏水,则说明该容量瓶不漏水
(2)B (3)10.73%
解析

练习册系列答案
相关题目
下列是纯净物的是:( )
| A.铝热剂 | B.酒精 | C.植物油 | D.淀粉 |
分类是化学学习和研究的常用手段。下列分类依据和结论都正确的是( )
| A.HCOOH、H2CO3、H2SO4分子中均含有两个氢原子,都是二元酸 |
| B.H2O、CH3COOH、CaCO3均含有氧元素,都是氧化物 |
| C.HCl、CH3COOH、CH3CH2OH都易溶于水,都是电解质 |
| D.HNO3、浓硫酸都具有强氧化性,都是氧化性酸 |
 Fe3O4 + nA↑+ 6S
Fe3O4 + nA↑+ 6S
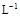 (NH4)2Fe(SO4)2 溶液充分反应,过量Fe2+再用0.0500 mol·
(NH4)2Fe(SO4)2 溶液充分反应,过量Fe2+再用0.0500 mol·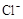 +5Fe3+ +2H2O
+5Fe3+ +2H2O 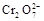 +6 Fe2+ =2Cr3+ + 6 Fe3+ +7H2O
+6 Fe2+ =2Cr3+ + 6 Fe3+ +7H2O