题目内容
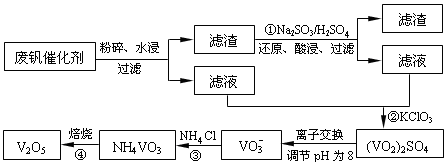
粗铜精炼后的阳极泥含有Cu、Au(金)和PbSO4等杂质,湿法处理阳极泥进行综合利用的流程如下:
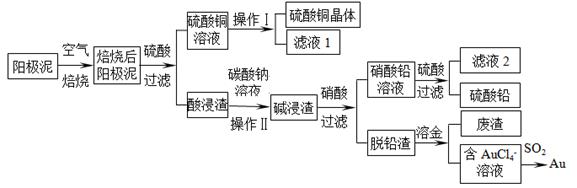
(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有: 和Cu-2e-= Cu2+。
(2)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是 ,焙烧后的阳极泥中除含金、PbSO4外,还有 (填化学式)。
(3)操作I的主要步骤为 ,操作Ⅱ的名称是 。
(4)写出用SO2还原AuCl4-的离子方程式 。
(5)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法 。
(6)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)= 1.82×10-8,用离子方程式表示加入碳酸钠溶液的作用 。

(1)用CuSO4做电解液电解含铜、金、铅的粗铜,阳极的电极反应式有: 和Cu-2e-= Cu2+。
(2)焙烧阳极泥时,为了提高焙烧效率,采取的合理措施是 ,焙烧后的阳极泥中除含金、PbSO4外,还有 (填化学式)。
(3)操作I的主要步骤为 ,操作Ⅱ的名称是 。
(4)写出用SO2还原AuCl4-的离子方程式 。
(5)为了减少废液排放、充分利用有用资源,工业上将滤液1并入硫酸铜溶液进行循环操作,请指出流程图中另一处类似的做法 。
(6)已知298K时,Ksp(PbCO3)=1.46×10-13,Ksp(PbSO4)= 1.82×10-8,用离子方程式表示加入碳酸钠溶液的作用 。
(1)Pb-2e-+SO42-=PbSO4 (2分)(答Pb-2e-=Pb2+得1分)
(2)将阳极泥粉碎,逆流焙烧等(2分) CuO (2分)
(3)蒸发浓缩,降温结晶,过滤。(或继续)洗涤,干燥(2分) 过滤(2分)
(4)2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+ (3分)
(5)用滤液2溶解碱浸渣 (或并入硝酸中)。(2分)(利用滤液2,但循环错误的,扣1分)
(6)PbSO4(s)+CO32-(aq) PbCO3(s)+SO42-(aq) (2分,用“=”不扣分)
PbCO3(s)+SO42-(aq) (2分,用“=”不扣分)
(2)将阳极泥粉碎,逆流焙烧等(2分) CuO (2分)
(3)蒸发浓缩,降温结晶,过滤。(或继续)洗涤,干燥(2分) 过滤(2分)
(4)2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+ (3分)
(5)用滤液2溶解碱浸渣 (或并入硝酸中)。(2分)(利用滤液2,但循环错误的,扣1分)
(6)PbSO4(s)+CO32-(aq)
 PbCO3(s)+SO42-(aq) (2分,用“=”不扣分)
PbCO3(s)+SO42-(aq) (2分,用“=”不扣分)试题分析:(1电解精炼的粗铜作阳极会发生氧化反应,其中单质铜和活性的金属都会发生溶解,因此粗铜中的铜和铅会发生失电子的氧化反应,电极反应式为:Pb-2e-+SO42-=PbSO4。
(2)由题干可知,用于焙烧的阳极泥的成分为Cu、Au(金)和PbSO4 等,所以在被烧过程中铜被氧化为了CuO,而Au(金)和PbSO4 均较稳定。要使焙烧效率提高,合理措施是把得到的阳极泥充分的粉碎,增大接触面积,或把反应后的气体在次逆流焙烧,这样可以升高温度且减少能耗。
(3)操作I的步骤是从硫酸铜溶液中获得硫酸铜晶体,因此该步骤是蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤。操作II是从酸浸渣(PbSO4)中得到碱浸渣(PbCO3),因此该操作是过滤操作。
(4)SO2还原AuCl4- 中还原剂和氧化剂都比较明确,因此很容易推测出氧化产物是SO42-,还原产物是Au。因此根据氧化还原反应得失电子守恒先缺项配平,然后根据电荷守恒再配平,因此得到的反应方程式为:2AuCl4-+3SO2+6H2O=2Au+3SO42-+8Cl-+12H+ 。
(5)滤液1是在结晶硫酸铜时剩下的滤液,还含有少量的未析出的硫酸铜,因此并入前面的硫酸铜溶液进行循环,有利于充分利用。因此类似此处的做法,应该是流程中得到的另一滤液2。此滤液2是在硝酸铅溶液中加入硫酸生成硫酸铅沉淀并过滤走硫酸铅后剩下的溶液,此溶液中H+没有发生反应,因此还有大量的硝酸溶液,所以可以把此滤液当成硝酸加入前面的碱浸渣中溶解碱浸渣,或者与前面碱浸渣步骤需要加入的硝酸合并加以利用。
(6)通过比较两种沉淀的溶度积,可以看出碳酸铅比硫酸铅更加难溶,因此往硫酸铅中加入碳酸钠,发生的是沉淀溶解转化的反应,所以离子方程式要注意标明状态,最好弄可逆号,所以方程式为:PbSO4(s)+CO32-(aq)
 PbCO3(s)+SO42-(aq)。
PbCO3(s)+SO42-(aq)。
练习册系列答案
相关题目
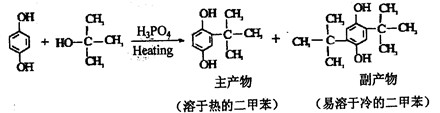

 )如下:
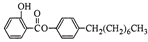
)如下: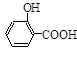 (水杨酸)+SOCl2→
(水杨酸)+SOCl2→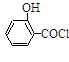 (水杨酰氯)+HCl↑+SO2↑
(水杨酰氯)+HCl↑+SO2↑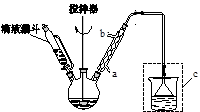
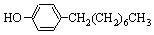 ),温度控制在100℃左右,不断搅拌。
),温度控制在100℃左右,不断搅拌。