题目内容
【题目】A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B元素的最高价氧化物的水化物与其简单氢化物能相互反应生成盐;C元素原子的最外层电子数是内层电子数的3倍;D元素的主族序数等于其周期数;E元素原子的最外层电子数是其电子层数的2倍。G单质是日常生活中用量最大的金属,易被腐蚀。
试回答下列问题:
(1)A元素的同位素有___________(写原子符号)
(2)实验室制取B的简单氢化物的化学反应方程式为_________________________
(3)C、D、E、F的简单离子半径由大到小的顺序是_________________(用离子符号表示)
(4)用化学事实说名E与F这两种元素非金属性的强弱_____________________(举一例)
(5)下列有关G的说法不正确的是_______
A、铁位于第四周期ⅧB族,在人体内的血红蛋白中含有铁元素
B、过量的铁分别与氯气和稀盐酸反应所得氯化物相同
C、FeCl3、FeCl2、Fe(OH)3都可以通过化合反应制取
D、氢氧化铁与HI溶液仅发生中和反应
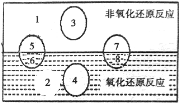
(6)向NaOH溶液中通入一定量的F单质,两者恰好完全反应,生成物中有三种含F的离子,其中两种离子的物质的量与反应时间的曲线如图所示。请写出t2时反应的总的化学方程式 _____________________ 。

【答案】(1)1H2H3H或H D T
(2)2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O
(3) S2- >Cl->O2-> Al3+;
(4)与H2化合Cl2比S容易;或:HCl比H2S要稳定;或:2H2S+Cl2 =2S+2HCl(任意一例)
(5)ABD
(6)5Cl2+10 NaOH=7NaCl+2NaClO+NaClO3+5H2O
【解析】试题分析:A是周期表中原子半径最小的元素,A是H;B元素的最高价氧化物的水化物与其简单氢化物能相互反应生成盐,B是N;C元素原子的最外层电子数是内层电子数的3倍,C是O;D元素的主族序数等于其周期数,D是Al;E元素原子的最外层电子数是其电子层数的2倍,E是S。F是Cl;G单质是日常生活中用量最大的金属,易被腐蚀,G是Fe。
(1)A元素的同位素有1H2H3H
(2)实验室制取氨气的化学反应方程式为2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O
2NH3↑+CaCl2+2H2O
(3)电子层数越多半径越大、电子层数相同时,质子数越多半径越小,离子半径由大到小的顺序是S2- >Cl->O2-> Al3+
(4)2H2S+Cl2 =2S+2HCl,说明氯元素非金属性比硫的强。
(5)下列有关G的说法不正确的是_______
A、铁位于第四周期Ⅷ族,在人体内的血红蛋白中含有铁元素;
B、过量的铁分别与氯气生成氯化铁,铁与稀盐酸反应生成氯化亚铁;
C、铁与氯气化合生成FeCl3、氯化铁与铁化合生成FeCl2、氢氧化亚铁和氧气和水化合才Fe(OH)3;
D、氢氧化铁与HI溶液发生氧化还原反应、中和反应
(6)向NaOH溶液中通入一定量的F单质,两者恰好完全反应,生成物中有三种含F的离子,其中两种离子的物质的量与反应时间的曲线如图所示。根据氧化还原反应规律, t2时生成物中有三种含Cl的离子是氯离子、次氯酸根离子、氯酸根离子,反应的总的化学方程式5Cl2+10 NaOH=7NaCl+2NaClO+NaClO3+5H2O。

 阅读快车系列答案
阅读快车系列答案