题目内容
【题目】用下列方法均可制得氧气:
①2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
②2HgO![]() 2Hg+O2↑
2Hg+O2↑
③2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
④2H2O2![]() 2H2O+O2↑
2H2O+O2↑
若要制得相同质量的氧气,反应中电子转移数目之比为( )
A.1:1:1:1B.2:2:2:1C.3:1:1:1D.2:1:1:1
【答案】B
【解析】
若要制得相同质量的氧气,假设都制1mol氧气,则①2KClO3![]() 2KCl+3O2↑,KClO3中2价氧升高变为0价,则1mol氧气转移4mol电子;②2HgO
2KCl+3O2↑,KClO3中2价氧升高变为0价,则1mol氧气转移4mol电子;②2HgO![]() 2Hg+O2↑,HgO中2价氧升高变为0价,则1mol氧气转移4mol电子;③2KMnO4
2Hg+O2↑,HgO中2价氧升高变为0价,则1mol氧气转移4mol电子;③2KMnO4![]() K2MnO4+MnO2+O2↑,KMnO4中2价氧升高变为0价,则1mol氧气转移4mol电子;④2H2O2
K2MnO4+MnO2+O2↑,KMnO4中2价氧升高变为0价,则1mol氧气转移4mol电子;④2H2O2![]() 2H2O+O2↑,H2O2中1价氧升高变为0价,则1mol氧气转移1mol电子;因此反应中电子转移数目之比为4:4:4:2 =2:2:2:1;故B符合题意。
2H2O+O2↑,H2O2中1价氧升高变为0价,则1mol氧气转移1mol电子;因此反应中电子转移数目之比为4:4:4:2 =2:2:2:1;故B符合题意。
综上所述,答案为B。

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
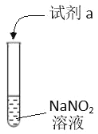
【题目】利用下列实验探究亚硝酸钠(NaNO2)的化学性质(AgNO2是淡黄色难溶于水的固体)
实验 | 装置 | 试剂a | 现象 |
① |
| 酚酞 | 无色溶液变红 |
② | AgNO3溶液 | 产生淡黄色沉淀 | |
③ | 淀粉KI 溶液+稀硫酸 | 无色溶液立即变蓝 | |
④ | 酸性K2Cr2O7溶液 | 无色溶液变为绿色 |
由上述实验所得结论不正确的是
A.NaNO2溶液呈碱性:NO2-+H2OHNO2+OH-
B.NaNO2可与某些盐发生复分解反应:NO2-+Ag+=AgNO2↓
C.NaNO2有氧化性:2I-+2H++2NO2-=I2+2NO2↑+H2O
D.NaNO2有还原性:Cr2O72-+3NO2-+8H+=3NO3-+2Cr3++4H2O