题目内容
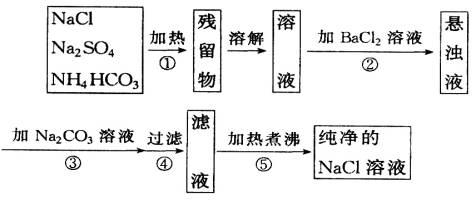
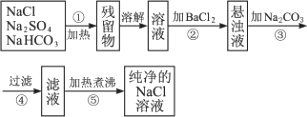
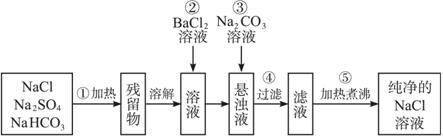
为了将混有Na2SO4、NaHCO3的NaCl提纯,并制得纯净的NaCl溶液,某学生设计了如图所示的实验方案:

(1)操作①盛放药品可选用________.(填仪器名称)
(2)操作②为什么不用Ba(NO3)2溶液,其理由是________.
(3)进行操作②后,如何判断SO![]() 已除尽?方法是________.
已除尽?方法是________.
(4)操作③的目的是________;为何不先过滤后加Na2CO3溶液,其理由是________.
(5)此设计方案是否严密?请说明理由________.
答案:
解析:
解析:
|
答案:(1)坩埚;(2)会引入NO 思路解析:根据题目信息可知欲提纯NaCl,则需除去其中含有的杂质硫酸钠和碳酸氢钠,根据转化关系知①主要是使碳酸氢钠分解,②中则是除去碳酸根离子和硫酸根离子,但需要提纯NaCl,所以加入硝酸钡容易引入新的杂质离子硝酸根离子,故选用氯化钡. |

练习册系列答案
相关题目