��Ŀ����
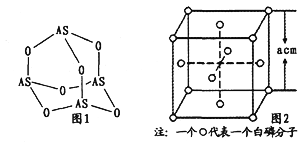
����Ŀ���л���A���������Ƿ��͵õ���Ҳ�ɴ���ţ������ȡ��������AΪ��ɫ��Һ�壬������ˮ��Ϊ�о�A�������ṹ������������ʵ�飺
��1����ȡA 9.0g������ʹ�������������ܶ�����ͬ������H2��45����ʵ����ۣ�A����Է�������Ϊ_____��
��2����9.0g A������O2�г��ȼ�գ���ʹ��������λ���ͨ������Ũ���ᡢ��ʯ�ң��������߷ֱ�����5.4g��13.2g����A�ķ���ʽΪ_____��
��3����ȡA 9.0g����������NaHCO3��ĩ��Ӧ������2.24L CO2����״�������������������Ʒ�Ӧ������2.24L H2����״������
ʵ����ۣ�A�к��еĹ����ţ����ƣ���_____��
��4��A�ĺ˴Ź���������ͼ��ʵ����ۣ�A�к���_____����ԭ����
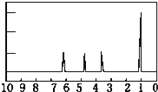
��5������������A�Ľṹ��ʽΪ_____��
���𰸡� 90 C3H6O3 �Ȼ����ǻ� 4 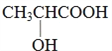
��������(1)�����ܶ�����ͬ������H2��45������֪A����Է�������Ϊ45��2=90���ʴ�Ϊ��90��
(2)���������֪��n(A)= ![]() =0.1mol��n(C)=n(CO2)=
=0.1mol��n(C)=n(CO2)= ![]() =0.3mol��n(H)=2n(H2O)=2��
=0.3mol��n(H)=2n(H2O)=2��![]() =0.6mol��n(O)=
=0.6mol��n(O)= ![]() =0.3mol������A�ķ���ʽΪ��C3H6O3���ʴ�Ϊ��C3H6O3��
=0.3mol������A�ķ���ʽΪ��C3H6O3���ʴ�Ϊ��C3H6O3��
(3)0.1molA��NaHCO3��Ӧ�ų�0.1molCO2����˵A��Ӧ����һ���Ȼ����������������Ʒ�Ӧ������0.1molH2��˵��A�л�����һ���ǻ����ʴ�Ϊ���Ȼ����ǻ���
(4)�˴Ź�����������4�����շ壬���֮��Ϊ1��1��1��3����֪A��Ӧ����4�ֲ�ͬ��������ԭ�ӣ��ʴ�Ϊ��4��
(5)����������A�Ľṹ��ʽΪ��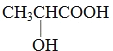 ���ʴ�Ϊ��
���ʴ�Ϊ��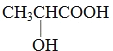 ��
��

 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�����Ŀ�������±��й������ܻ�������ܶȻ����й�˵����ȷ����
������ | �ܶȻ���25���� | ������ | �ܶȻ���25���� |
FeCO3 | 3.2��10��11 | Fe(OH)3 | 4.0��10��38 |
Fe(OH)2 | 8.0��10��11 | FeS | 6.3��10��18 |
A. ��c(CO32-)=0.1 mol��L-1����Һ�У�c(Fe2+)��3.2��10-10 mol��L-1
B. ��FeCl3�� FeCl2��Һ�ֱ����PH=10����c(Fe2+)< c(Fe3+)
C. ������Һ�����ԣ������ڽ�Fe2+����ΪFeS��FeCO3
D. ����ӦҺ�е�Fe2+����Ϊ Fe3+�����ڽ�������Һ�г���