题目内容
16.下列物质既能与盐酸反应,又能与烧碱溶液反应的是( )①Al2O3 ②Al(OH)3 ③Al ④NaHCO3 ⑤NaHS ⑥CaCO3 ⑦NaHSO4 ⑧(NH4)2CO3.
| A. | 除⑥外 | B. | 除⑥、⑦外 | C. | 除⑥、⑦、⑧外 | D. | 除①、②、③、④、⑤外 |
分析 既能够与酸反应又能够与碱反应的物质有:铝;两性物质;弱酸的酸式盐,弱酸对应铵盐,据此解答.
解答 解:①Al2O3 是两性氧化物,既能与盐酸反应又能与氢氧化钠反应,故选;
②Al(OH)3 是两性氢氧化物,既能与盐酸反应又能与氢氧化钠反应,故选;
③Al 既能与盐酸反应又能与氢氧化钠反应,故选;
④NaHCO3 是弱酸的酸式盐,既能与盐酸反应又能与氢氧化钠反应,故选;
⑤NaHS 是弱酸的酸式盐,既能与盐酸反应又能与氢氧化钠反应,故选;
⑥CaCO3 与氢氧化钠不反应,故不选;
⑦NaHSO4 与盐酸不反应,故不选;
⑧(NH4)2CO3弱酸对应铵盐,既能与盐酸反应又能与氢氧化钠反应,故选;
故选:B.
点评 本题考查了物质的性质,明确能和强酸或强碱反应的物质是解本题的关键,注意相关知识的积累.

练习册系列答案
相关题目
6.下列说法正确的是( )
| A. | 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ•mol-1,则H2O(g)?H2O(l) 的△H=+40.69 kJ•mol-1 | |||||||||||||||
| B. | 已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)•c(CO32-)=6.82×10-6 | |||||||||||||||
| C. | 已知某些化学键的键能数据如下表:
| |||||||||||||||
| D. | 常温下,在0.10 mol•L-1的NH3•H2O溶液中加入少量NH4Cl晶体,能使NH3•H2O的电离度降低,溶液的pH减小 |
7.下列关于丙烯(CH3-CH=CH2)的说法正确的是( )
| A. | 丙烯分子有8个σ键,1 个π键 | |
| B. | 丙烯分子中3个碳原子都是sp3杂化 | |
| C. | 丙烯分子不存在非极性键 | |
| D. | 丙烯分子中3个碳原子可能在同一直线上 |
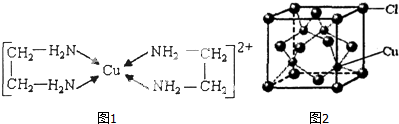
11.已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中A、B、C是同一周期的非金属元素.化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2:1,三个氯离子位于外界.请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为C<O<N.
(2)B的氢化物的分子空间构型是三角锥型.其中心原子采取sp3杂化.
(3)写出化合物AC2的电子式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
(4)ECl3与B、C的氢化物形成配位数为六的配合物的化学式为[Cr(NH3)4(H2O)2]Cl3.
| X | ||
| Y | ||
| Z |
(2)B的氢化物的分子空间构型是三角锥型.其中心原子采取sp3杂化.
(3)写出化合物AC2的电子式
 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.
;一种由B、C组成的化合物与AC2互为等电子体,其化学式为N2O.(4)ECl3与B、C的氢化物形成配位数为六的配合物的化学式为[Cr(NH3)4(H2O)2]Cl3.
5.下列物质肯定为纯净物的是( )
| A. | 汽油 | B. | C2H6O | C. | 聚乙烯 | D. | 甘油 |
6.下列除去杂质的方法正确的是( )
| A. | 除去乙烷中少量的乙烯:光照条件下通入Cl2,使乙烯转化成液态二氯乙烷而与乙烷分离 | |
| B. | 除去乙醇中少量的乙酸:加足量生石灰,蒸馏 | |
| C. | 除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶 | |
| D. | 除去乙酸乙酯中少量的乙酸:用氢氧化钠溶液洗涤,分液、干燥、蒸馏 |
 乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔.
乙炔是有机合成工业的一种原料.工业上曾用CaC2与水反应生成乙炔. ;1mol O22+中含有的π键数目为2NA个.
;1mol O22+中含有的π键数目为2NA个.