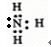��Ŀ����
��12�֣�X��Y��Z��L��M����Ԫ�ص�ԭ��������������X��Y��Z��L����ɵ����ʵĻ���Ԫ�أ�M�ǵؿ��к�����ߵĽ���Ԫ�ء��ش��������⣺
(1) L�Ĺ����ʾʽΪ________��
(2)����Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳����____________________����Ԫ�ط��ű�ʾ����
(3)Z��X��Ԫ�ذ�ԭ����Ŀ��l��3��2��4���ɷ���A��B��A�ķ��ӿռ乹��Ϊ____________��A�ĵ���ʽΪ____________��B�ĽṹʽΪ____________��
(4) ����se��������������Ԫ�أ���Lͬһ���壬Seԭ�ӱ�Lԭ�Ӷ��������Ӳ㡣����2-- 5����Ԫ�ص��ʷֱ���H2��Ӧ����l mol��̬�⻯��ķ�Ӧ�����£���ʾ����1 mol�����ⷴӦ�ȵ���__________������ĸ���ţ���
a��+99.7 kJ��mol��1 b��+29.7kJ��mol��1
c����20.6 kJ��mol��1 d����241.8 kJ��mol��1
(5)��ҵ�ϳ��õ��M2L3�ķ�������ȡM���ʡ����Ƶ�54��M����ʱ��ת�Ƶ��ӵ����ʵ�����___________ mol
��12�֣�(1)O�Ĺ����ʾʽ:�ԣ�2�֣�
(2) Al��C��N��O��H��2�֣�
(3) ������ ��1�֣� ![]() ��1�֣�
��1�֣���2�֣�
(4) b��2�֣�
(5) 6 mol��2�֣�
����:

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�