��Ŀ����
����Ŀ����������һ�������ĩ�����п��ܺ��������������ʣ�![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ����֪
����֪![]() ������ˮ��
������ˮ��![]() ��Һ����ɫ���ֽ�������ʵ�飺
��Һ����ɫ���ֽ�������ʵ�飺
������ˮ����ɫ��Һ��������Һ�м���![]() ��Һ���ɰ�ɫ�������ټ�����ʱ������ʧ��
��Һ���ɰ�ɫ�������ټ�����ʱ������ʧ��
��������ʵ�������ƶϣ�
��1��һ�������ڵ������ǣ���д��ѧʽ��_________________________��
��2��һ�����ڵ������ǣ���д��ѧʽ��_________________________��
��3�����ܴ��ڵ������ǣ���д��ѧʽ��_________________________��
��4��������ܴ��ڵ����������Լ�����Ϊ��_________________________��
����5�����ǻ��õļ����Ԫ�أ��Ƽ��仯�������������������й㷺��Ӧ�á��ƼغϽ���ں˷�Ӧ���������Ƚ���Һ��![]() �ƼغϽ�����
�ƼغϽ�����![]() ˮ����
ˮ����![]() ������ȷ������-�غϽ����ɣ���
������ȷ������-�غϽ����ɣ���![]() ����ʽ��ʾ����__________�����������Һ�������Ϊ
����ʽ��ʾ����__________�����������Һ�������Ϊ![]() ����
����![]() ��Һ�����ʵ���Ũ��Ϊ___________________��
��Һ�����ʵ���Ũ��Ϊ___________________��
���𰸡�CaCO3��Na2SO4��CuSO4 Na2CO3 NaCl ϡ���ᡢ��������Һ NaK2 0.2mol/L
��������
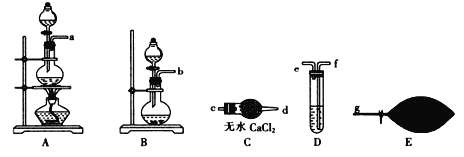
�����ɢ�����ˮ����ɫ��Һ����֪һ������CuSO4��CaCO3���ɢ�����Һ�м���BaCl2��Һ���ɰ�ɫ�������ټ�����ʱ������ʧ����֪��ɫ����Ϊ̼�ᱵ����һ����Na2CO3������Na2SO4������ȷ���Ƿ�NaCl���Դ�����𣻣�II�����ݷ�����Ӧ��2Na+2H2O=2NaOH+H2����2K+2H2O=2KOH+H2��������������������������з��̼���Na��K���ʵ���������![]() ����ɵá�
����ɵá�
�ɢ�����ˮ����ɫ��Һ����֪һ������CuSO4��CaCO3���ɢ�����Һ�м���BaCl2��Һ���ɰ�ɫ�������ټ�����ʱ������ʧ����֪��ɫ����Ϊ̼�ᱵ����һ����Na2CO3������Na2SO4������ȷ���Ƿ�NaCl��
��1��һ�������ڵ�������CaCO3��Na2SO4��CuSO4���ʴ�Ϊ��CaCO3��Na2SO4��CuSO4��
��2��һ�����ڵ�������Na2CO3���ʴ�Ϊ��Na2CO3��
��3�����ܴ��ڵ�������NaCl���ʴ�Ϊ��NaCl��
��4���������ӵļ��鷽����֪��������ܴ��ڵ����������Լ�Ϊϡ���ᡢ��������Һ���ʴ�Ϊ��ϡ���ᡢ��������Һ��
��5�����ơ��ص����ʵ����ֱ�Ϊamol��bmol����

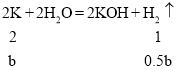
0.5a+0.5b=0.15��23a+39b=10.1������ɵã�a=0.10��b=0.20��n��Na����n��K��=1��2������-�غϽ�ѧʽΪNaK2��c(NaOH)=![]() ���ʴ�Ϊ��NaK2��0.2mol/L��
���ʴ�Ϊ��NaK2��0.2mol/L��

 �±�Сѧ��Ԫ�Բ���ϵ�д�
�±�Сѧ��Ԫ�Բ���ϵ�д� �ִʾ��ƪϵ�д�
�ִʾ��ƪϵ�д�����Ŀ����֪��ѧ��Ӧ����Fe(s)��CO2(g)![]() FeO(s)��CO(g)����ƽ�ⳣ��ΪK1����ѧ��Ӧ����Fe(s)��H2O(g)
FeO(s)��CO(g)����ƽ�ⳣ��ΪK1����ѧ��Ӧ����Fe(s)��H2O(g)![]() FeO(s)��H2(g)����ƽ�ⳣ��ΪK2�����¶�973 K��
FeO(s)��H2(g)����ƽ�ⳣ��ΪK2�����¶�973 K��
1173 K����£�K1��K2��ֵ�ֱ����£�
�¶� | K1 | K2 |
973 K | 1.47 | 2.38 |
1173 K | 2.15 | 1.67 |
(1)ͨ�������е���ֵ�����ƶϣ���Ӧ����________(��������������������)��Ӧ��
(2)���з�Ӧ����CO2(g)��H2(g)![]() CO(g)��H2O(g)������д���÷�Ӧ��ƽ�ⳣ��K3����ѧ����ʽ��K3��_________��
CO(g)��H2O(g)������д���÷�Ӧ��ƽ�ⳣ��K3����ѧ����ʽ��K3��_________��
(3)���жϷ�Ӧ���Ѵ�ƽ��״̬����_________��
A��������ѹǿ����
B�����������c(CO)����
C��v��(H2)��v��(H2O)
D��c(CO2)��c(CO)
(4)���ݷ�Ӧ���������Ƶ���K1��K2��K3֮��Ĺ�ϵʽ_________���ݴ˹�ϵʽ���ϱ����ݣ�Ҳ���ƶϳ���Ӧ����____________(��������������������)��Ӧ��Ҫʹ��Ӧ����һ�������½�����ƽ��������Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��_______(��д���)��
A����С��Ӧ�����ݻ� B������Ӧ�����ݻ�
C�������¶� D�������¶�
E��ʹ�ú��ʵĴ��� F���跨����CO����
����Ŀ������̿��ԭ��Ҳ���Դ������������ij�ܱ������м��������Ļ���̿��һ����NO��������ӦC(s) + 2NO(g)![]() N2(g) + CO2(g) + Q��Q��0������T1��ʱ����Ӧ���е���ͬʱ�䣬��������ڸ����ʵ����ʵ���Ũ�����£�
N2(g) + CO2(g) + Q��Q��0������T1��ʱ����Ӧ���е���ͬʱ�䣬��������ڸ����ʵ����ʵ���Ũ�����£�
ʱ�� /min | 0 | 10 | 20 | 30 | 40 | 50 | |
Ũ�� /mol��L-1 | NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 | |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 | |
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ________��0-10 min��NO��ƽ����Ӧ����Ϊ____________��
��30 min��ֻ�ı�ijһ���������ݱ��������жϸı������������__________����Ӧ�أ�ƽ��__��ѡ���ţ���
a��������Ӧ�����ƶ� b�����淴Ӧ�����ƶ� c���������ƶ�