��Ŀ����
A��B��C��D��Ԫ�����ڱ�ǰ�����ڳ���������Ԫ�أ�ԭ�������������� ���ǵ���ؽṹ��������Ϣ���±���ʾ�����������Ϣ�������ص����⣺
|
Ԫ�� ��ؽṹ������ A AΪ�ǽ���Ԫ�أ���һ�ֵ����ǵ�������壬���ۡ������������ԣ��������缫���� B �ǵ����ʵ����Ԫ��֮һ��ԭ�Ӻ��������ֲ�ͬ�����ĵ��ӣ���δ�ɶԵ�������� C �䵥�ʼ�����ǿ����ҺӦ������ǿ����Һ��Ӧ����������ڵ������ڵ��������а뾶��С D D�ĸ��Ȼ��������Һ������ӡˢ��·����·�ġ���ʴ�� |
��1��Dλ��Ԫ�����ڱ��� ���ڵ� �壬���̬ԭ�Ӻ���۵����Ų�ʽΪ ��Ԫ��D�ĸ��Ȼ����γɵ�����Һ��ʴӡˢ��·���·��������Ӧ �����ӷ���ʽΪ ��
��2������BԪ���γɵ�Na3B�������� ���壨����ӡ�����ԭ�ӡ��������ӡ����� ����BԪ�ص���̬�⻯�K������ˮ��ԭ������Ϊ���Ǿ��Ǽ��Է���֮�⣬����Ϊ ��
��3��Ԫ��A��Ԫ��B��ȣ��ǽ����Խ�ǿ���� ����Ԫ�ط��ű�ʾ����������Ϊ�ж����߷ǽ�����ǿ�������ݵ��� ��
a��������A�ĵ��ʺ�B�ĵ���״̬��ͬ
b��������ԭ���γɵĹ��ۼ��й��õ��ӶԵ�ƫ��
c������������Ӧˮ���������ǿ��
d���������ᷴӦ�����׳̶�
��4����֪��5.4gԪ��C�ĵ��ʿ���Ԫ��D�ĵͼ������ﷴӦ���ų�346.2kJ����������д���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��1�� �� (1��) �� ��1�֣� 3d64s2 ��2�֣� 2Fe3++Cu = 2 Fe2+ + Cu2+ (2��)
��2������ ��2�֣� NH3��H2O���Ӽ�����γ���� ��2�֣�
��3�� N ��1�֣� b c (2��)
��4��2Al(s) +3FeO(s) = Al2O3(s) + 3Fe (s) ��H = -3462 kJ/mol (3��)
��������
����������������Ϣ��֪��A��B��C��D�ֱ�ΪC��N��Al��Fe��
��1��Feλ�����ڱ��������ڣ��ڢ��壬�۵����Ų�ʽΪ3d64s2��
��2��Na3NΪ���Ӿ��壻NH3������ˮ��Ҫԭ���ǿ�����ˮ�����γ������
��3��a���ǽ�����ǿ���뵥��״̬�أ�����
b���ǽ�����ǿ�ĶԵ��ӶԵ������������õ��Ӷ���ƫ���Ԫ�أ���ȷ
c������������Ӧˮ���������Խǿ��ǽ�����Խǿ����ȷ
d���ǽ�����ǿ�����ᷴӦ�����أ�����
��4���Ȼ�ѧ��Ӧ����ʽ����д��ע�����ʵ�״̬��
���㣺���⿼����Ԫ�ص��ƶϣ���������Ų�ʽ��д���Ȼ�ѧ��Ӧ����ʽ����д���ǽ���ǿ�����жϵ�֪ʶ���ѶȲ���

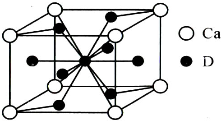 ��5�������Ͻ��������Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10-23 cm3��������γ�LaNinH4.5�Ͻ�����뾧����϶��������䣩����LaNin��n=
��5�������Ͻ��������Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10-23 cm3��������γ�LaNinH4.5�Ͻ�����뾧����϶��������䣩����LaNin��n=
