��Ŀ����
A��B��C��D��Ԫ�����ڱ��Ķ�����Ԫ�أ�������±���Ϣ�ش��������⣮
��1��B��Ԫ�����ڱ���λ��Ϊ
��2��A�����ڿ����г��ȼ�պ�IJ�����ˮ��Ӧ�Ļ�ѧ����ʽΪ
��3��д��D������������F�����ӷ���ʽ
��4������E��Һ�������ӵ�ʵ�鷽����
| Ԫ�� | A | B | C | D |
| ���� �ṹ ��Ϣ |
������������ȼ�ջ���ʻ�ɫ�������������̣����ò������������E���� ���ӵ�������ͬ�� |
�����Ǵ��н�������ĻҺ�ɫ���壬����Ϣ������ �ؼ����ϣ� |
����������ˮ����������̬�⻯�ﷴӦ�õ����ӻ�����E�� | ��������һ���ͻ���ϣ�������A������������ˮ����� ��������F�� |
�������ڡ��ڢ�A��
�������ڡ��ڢ�A��
����2��A�����ڿ����г��ȼ�պ�IJ�����ˮ��Ӧ�Ļ�ѧ����ʽΪ
2Na2O2+2H2O�T4NaOH+O2��
2Na2O2+2H2O�T4NaOH+O2��
����3��д��D������������F�����ӷ���ʽ
Al2O3+2OH-=2AlO2-+H2O
Al2O3+2OH-=2AlO2-+H2O
����4������E��Һ�������ӵ�ʵ�鷽����
�������Һ�м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ���飬����ֽ��������˵����Һ�д���NH4+
�������Һ�м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ���飬����ֽ��������˵����Һ�д���NH4+
��������A������������ȼ�ջ���ʻ�ɫ�������������̣�ӦΪNa��������ȼ�յ�������AΪNaԪ�أ�
B�����Ǵ��н�������ĻҺ�ɫ���壬����Ϣ�����Ĺؼ����ϣ���ΪSiԪ�أ�
C����������ˮ����������̬�⻯�ﷴӦ�õ����ӻ�����E����CΪNԪ�أ���������ΪNH4+��
D��������һ���ͻ���ϣ�������A������������ˮ����õ�������F����DΪAlԪ�أ�FΪNaAlO2��
����ԭ�ӵ�ԭ�ӽṹ�ص��Լ���Ӧ����������ʽ����⣮
B�����Ǵ��н�������ĻҺ�ɫ���壬����Ϣ�����Ĺؼ����ϣ���ΪSiԪ�أ�
C����������ˮ����������̬�⻯�ﷴӦ�õ����ӻ�����E����CΪNԪ�أ���������ΪNH4+��
D��������һ���ͻ���ϣ�������A������������ˮ����õ�������F����DΪAlԪ�أ�FΪNaAlO2��
����ԭ�ӵ�ԭ�ӽṹ�ص��Լ���Ӧ����������ʽ����⣮
����⣺A������������ȼ�ջ���ʻ�ɫ�������������̣�ӦΪNa��������ȼ�յ�������AΪNaԪ�أ�
B�����Ǵ��н�������ĻҺ�ɫ���壬����Ϣ�����Ĺؼ����ϣ���ΪSiԪ�أ�
C����������ˮ����������̬�⻯�ﷴӦ�õ����ӻ�����E����CΪNԪ�أ���������ΪNH4+��
D��������һ���ͻ���ϣ�������A������������ˮ����õ�������F����DΪAlԪ�أ�FΪNaAlO2��
��1��BΪSiԪ�أ�ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ4����λ�����ڱ��������ڡ��ڢ�A�壬
�ʴ�Ϊ���������ڡ��ڢ�A�壻
��2��A�����ڿ����г��ȼ�պ�IJ���ΪNa2O2����ˮ��Ӧ����NaOH��O2����Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2H2O�T4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2H2O�T4NaOH+O2����
��3��DΪAl����Ӧ��������ΪAl2O3��Ϊ�����������NaOH��Һ��Ӧ����NaAlO2��H2O��
��Ӧ�����ӷ���ʽΪAl2O3+2OH-=2AlO2-+H2O���ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��
��4��ʵ���Ҽ���NH4+����ʱ��������NH3�ļ��ԣ�һ���������������Һ�м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ���飬����ֽ��������˵����Һ�д���NH4+��
�ʴ�Ϊ���������Һ�м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ���飬����ֽ��������˵����Һ�д���NH4+��
B�����Ǵ��н�������ĻҺ�ɫ���壬����Ϣ�����Ĺؼ����ϣ���ΪSiԪ�أ�
C����������ˮ����������̬�⻯�ﷴӦ�õ����ӻ�����E����CΪNԪ�أ���������ΪNH4+��
D��������һ���ͻ���ϣ�������A������������ˮ����õ�������F����DΪAlԪ�أ�FΪNaAlO2��
��1��BΪSiԪ�أ�ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ4����λ�����ڱ��������ڡ��ڢ�A�壬
�ʴ�Ϊ���������ڡ��ڢ�A�壻
��2��A�����ڿ����г��ȼ�պ�IJ���ΪNa2O2����ˮ��Ӧ����NaOH��O2����Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2H2O�T4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2H2O�T4NaOH+O2����
��3��DΪAl����Ӧ��������ΪAl2O3��Ϊ�����������NaOH��Һ��Ӧ����NaAlO2��H2O��
��Ӧ�����ӷ���ʽΪAl2O3+2OH-=2AlO2-+H2O���ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��
��4��ʵ���Ҽ���NH4+����ʱ��������NH3�ļ��ԣ�һ���������������Һ�м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ���飬����ֽ��������˵����Һ�д���NH4+��
�ʴ�Ϊ���������Һ�м���ŨNaOH��Һ�����ȣ���ʪ��ĺ�ɫʯ����ֽ���飬����ֽ��������˵����Һ�д���NH4+��
���������⿼��Ԫ�ص��ƶϣ���Ŀ�Ѷ��еȣ�����ʱע��������ʵ������Լ���Ӧ�ĵ��������ƶ�Ԫ�ص����࣬ע��������Ԫ�ػ�����֪ʶ��

��ϰ��ϵ�д�
�����Ŀ
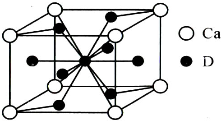 ��5�������Ͻ��������Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10-23 cm3��������γ�LaNinH4.5�Ͻ�����뾧����϶��������䣩����LaNin��n=
��5�������Ͻ��������Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10-23 cm3��������γ�LaNinH4.5�Ͻ�����뾧����϶��������䣩����LaNin��n=
