��Ŀ����
A��B��C��D��Ԫ�����ڱ���ǰ36��Ԫ�أ����ǵĺ˵�����������ڶ�����Ԫ��Aԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2����Bԭ�ӵ������P����ĵ���Ϊ������ṹ��C�ǵؿ��к�������Ԫ�أ�D�ǵ�������Ԫ�أ���ԭ�Ӻ�����������������ԭ����ͬ�����������Ӿ���������ش��������⣺
��1��A��B��C�ĵ�һ��������С�����˳���� ���ö�Ӧ��Ԫ�ط��ű�ʾ������̬Dԭ�ӵĵ����Ų�ʽΪ ��
��2��A������������Ӧ��ˮ��������У�������ԭ�Ӳ�ȡ �ӻ���BC3-�Ŀռ乹��Ϊ ����������������
��3��1mol AB-�к��еĦм�����Ϊ ��
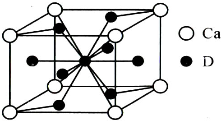
��4����ͼ�ǽ���Ca��D���γɵ�ij�ֺϽ�ľ����ṹʾ��ͼ����úϽ���Ca��D��ԭ�Ӹ����� ��
 ��5�������Ͻ��������Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10-23 cm3��������γ�LaNinH4.5�Ͻ�����뾧����϶��������䣩����LaNin��n= ������ֵ�������ںϽ��е��ܶ�Ϊ ��
��5�������Ͻ��������Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10-23 cm3��������γ�LaNinH4.5�Ͻ�����뾧����϶��������䣩����LaNin��n= ������ֵ�������ںϽ��е��ܶ�Ϊ ��
��1��A��B��C�ĵ�һ��������С�����˳����
��2��A������������Ӧ��ˮ��������У�������ԭ�Ӳ�ȡ
��3��1mol AB-�к��еĦм�����Ϊ
��4����ͼ�ǽ���Ca��D���γɵ�ij�ֺϽ�ľ����ṹʾ��ͼ����úϽ���Ca��D��ԭ�Ӹ�����
 ��5�������Ͻ��������Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10-23 cm3��������γ�LaNinH4.5�Ͻ�����뾧����϶��������䣩����LaNin��n=
��5�������Ͻ��������Ͻ�����ͬ���͵ľ����ṹXYn�������к�ǿ�Ĵ�����������֪�����Ͻ�LaNin�������Ϊ9.0��10-23 cm3��������γ�LaNinH4.5�Ͻ�����뾧����϶��������䣩����LaNin��n=������A��B��C��D����ǰ36��Ԫ�أ����ǵĺ˵������������C�ǵؿ��к�����ߵ�Ԫ�أ�����C��OԪ�أ�Bԭ�ӵ������p����ĵ���Ϊ�����ṹ�����������Ų�Ϊ2s22p3����BΪNԪ�أ��ڶ�����Ԫ��Aԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2������ԭ�Ӻ�������Ų�Ϊ1s22s1��1s22s22p2����ϣ�3������NԪ���γ������ӣ�AN-������AΪCԪ�أ�D�ǵ�������Ԫ�أ���ԭ�Ӻ�����������������ԭ����ͬ�����������Ӿ���������DԪ��ԭ�Ӹ���������ֱ�Ϊ2��8��18��1����29��CuԪ�أ��ݴ˽��
����⣺A��B��C��D����ǰ36��Ԫ�أ����ǵĺ˵������������C�ǵؿ��к�����ߵ�Ԫ�أ�����C��OԪ�أ�Bԭ�ӵ������p����ĵ���Ϊ�����ṹ�����������Ų�Ϊ2s22p3����BΪNԪ�أ��ڶ�����Ԫ��Aԭ�ӵĺ���ɶԵ�������δ�ɶԵ�������2������ԭ�Ӻ�������Ų�Ϊ1s22s1��1s22s22p2����ϣ�3������NԪ���γ������ӣ�AN-������AΪCԪ�أ�D�ǵ�������Ԫ�أ���ԭ�Ӻ�����������������ԭ����ͬ�����������Ӿ���������DԪ��ԭ�Ӹ���������ֱ�Ϊ2��8��18��1����29��CuԪ�أ�
��1��C��N��OԪ����ͬһ����Ԫ�أ�ͬһ����Ԫ��������ҵ�һ�����ܳ��������ƣ���NԪ��ԭ��2p�ܼ��ǰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ��ʵ�һ������C��O��N��
D��ԭ��������29��ΪCuԪ�أ���ԭ�Ӻ�������Ų�ʽΪ��1s22s22p63s23p63d104s1��
�ʴ�Ϊ��C��O��N��1s22s22p63s23p63d104s1��
��2��H2CO3��Cԭ������������ȫ���ɼ���û�йµ��Ӷԣ���1��C=O˫����2��C-O�������ӻ������ĿΪ3����ȡsp2�ӻ���NO3-��Nԭ���γ�3���ļ����µ��Ӷ�=
=0����ӦΪƽ�������Σ�
�ʴ�Ϊ��sp2��ƽ�������Σ�
��3����CN-��Cԭ�Ӽ�1������ɻ���1��Nԭ�ӣ��ɵõĵȵ�����N2��CN-���γ�C��N������1��CN-����2���м�����1mol CN-�к��еĦм�����Ϊ2NA��
�ʴ�Ϊ��2NA��
��4���ɾ����ṹ��֪��Caԭ�Ӵ��ڶ��㣬�����к���Caԭ����ĿΪ8��
=1��Cuԭ�Ӵ��ھ����ڲ������ϡ����ģ�������Cu��ĿΪ1+4��
+4��
=5���ʸúϽ���Ca��Cu��ԭ�Ӹ�����Ϊ1��5��
�ʴ�Ϊ��1��5��
��5���ɣ�4��֪n=5��������ӵ��4.5��Hԭ�ӣ����ںϽ��е��ܶ�Ϊ
=0.083g/cm3��
�ʴ�Ϊ��5��0.083g/cm3��
��1��C��N��OԪ����ͬһ����Ԫ�أ�ͬһ����Ԫ��������ҵ�һ�����ܳ��������ƣ���NԪ��ԭ��2p�ܼ��ǰ����ȶ�״̬�������ϵͣ���һ�����ܸ���ͬ��������Ԫ�أ��ʵ�һ������C��O��N��
D��ԭ��������29��ΪCuԪ�أ���ԭ�Ӻ�������Ų�ʽΪ��1s22s22p63s23p63d104s1��
�ʴ�Ϊ��C��O��N��1s22s22p63s23p63d104s1��
��2��H2CO3��Cԭ������������ȫ���ɼ���û�йµ��Ӷԣ���1��C=O˫����2��C-O�������ӻ������ĿΪ3����ȡsp2�ӻ���NO3-��Nԭ���γ�3���ļ����µ��Ӷ�=
| 5+1-3��2 |
| 2 |
�ʴ�Ϊ��sp2��ƽ�������Σ�
��3����CN-��Cԭ�Ӽ�1������ɻ���1��Nԭ�ӣ��ɵõĵȵ�����N2��CN-���γ�C��N������1��CN-����2���м�����1mol CN-�к��еĦм�����Ϊ2NA��
�ʴ�Ϊ��2NA��
��4���ɾ����ṹ��֪��Caԭ�Ӵ��ڶ��㣬�����к���Caԭ����ĿΪ8��
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 2 |
�ʴ�Ϊ��1��5��
��5���ɣ�4��֪n=5��������ӵ��4.5��Hԭ�ӣ����ںϽ��е��ܶ�Ϊ
| ||
| 9.0��10-23cm3 |
�ʴ�Ϊ��5��0.083g/cm3��
������������Ԫ�ص��ƶ�Ϊ���壬�����˵����ܡ��ӻ����ۣ����ӽṹ����������Ų����ɡ����������֪ʶ�㣬�Ƕ����ʽṹ֪ʶ���ۺϿ��飬���ض�֪ʶǨ�Ƶ����á��������������������飬ע��ͬһ����Ԫ�صĵ�һ����������ԭ�����������������������ƣ�����IIA�͵�IIIA�塢��VA��͵�VIA��֮���쳣��

��ϰ��ϵ�д�
�����Ŀ

