题目内容
6. 如图为元素周期表中短周期的一部分,下列有关X、Y、Z、W、T五种元素的叙述中错误的是( )
如图为元素周期表中短周期的一部分,下列有关X、Y、Z、W、T五种元素的叙述中错误的是( )| A. | X与Y形成的阴离子只有XY32- | |
| B. | Z元素的最高价氧化物对应水化物的酸性最强 | |
| C. | 六种元素分别形成的单质晶体中,X的熔、沸点可能最高 | |
| D. | 这五种元素两两组合,形成只有极性键的非极性分子的物质数大于3 |
分析 由元素在短周期中的位置,可知X为C元素,Y为O元素,Z为F元素,W为S元素,T为Cl.
A.C、O元素阴离子有CO32-、C2O42-等;
B.F元素没有最高价含氧酸;
C.碳元素可以形成原子晶体,其元素形成分子晶体;
D.五种元素两两组合,形成只有极性键的非极性分子的物质有CH4、CCl4、CF4、CO2、CS2.
解答 解:由元素在短周期中的位置,可知X为C元素,Y为O元素,Z为F元素,W为S元素,T为Cl.
A.C、O元素阴离子有CO32-、C2O42-等,故A错误;
B.最高价含氧酸酸性最强的为高氯酸,而F元素没有最高价含氧酸,故B错误;
C.碳元素可以形成原子晶体,其它元素形成分子晶体,故碳元素形成晶体熔沸点最高,故C正确;
D.五种元素两两组合,形成只有极性键的非极性分子的物质有CH4、CCl4、CF4、CO2、CS2,故D正确,
故选AB.
点评 本题考查元素周期表的综合应用,A选项为易错点,学生容易忽略有机酸,难度中等.

练习册系列答案
相关题目
16.某未知溶液可能含Cl-、CO32-、Na+、SO42-、Al3+.将溶液滴在蓝色石蕊试纸上,试纸变红.取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀.下列判断合理的是( )
| A. | 可能有Cl-和SO42- | B. | 一定有Al3+ 和SO42- | ||
| C. | 可能有Al3+ 和Cl- | D. | 一定没有CO32- |
14.结构片段为…-CH2-CH=CH-CH2-…的高分子化合物的单体是( )
| A. | 乙烯 | B. | 乙炔 | C. | 正丁烯 | D. | 1,3-丁二烯 |
1.分子式为CnH2nO2的羧酸和某醇发生酯化反应生成分子式为Cn+6H2n+12O2的酯,反应所需羧酸和醇的质量比为1:1,则该羧酸的同分异构体中属于酯的有( )
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 12种 |
10.下列变化属于化学变化的是( )
| A. | 碘的升华 | B. | 用CCl4萃取溴水中的溴 | ||
| C. | AgBr感光 | D. | 浓盐酸的挥发 |
7.结构简式为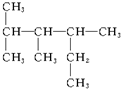 的物质,其名称是( )
的物质,其名称是( )
 的物质,其名称是( )
的物质,其名称是( )| A. | 2,3,4-三甲基己烷 | B. | 1,1,2-三甲基-3-乙基丁烷 | ||
| C. | 2-乙基-3,4-二甲基戊烷 | D. | 3,4,5-三甲基己烷 |
8.等温等压下,关于等质量H2、D2、T2三种气体的下列叙述中正确的是( )
| A. | 密度之比1:2:3 | B. | 质子数之比6:3:2 | C. | 中子数之比0:3:4 | D. | 体积之比6:3:2 |