题目内容
8.下列说法不正确的是( )| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 两种不同的非金属元素形成的化合物中只存在极性共价键 | |
| C. | 共价化合物不可能存在离子键 | |
| D. | 某元素原子最外层只有1个电子,它跟卤素可能形成离子键也可能形成共价键 |
分析 A.含有离子键的化合物是离子化合物,离子化合物中可能含有共价键;
B.两种不同的非金属元素形成的化合物中可能存在极性键和非极性键;
C.只含共价键的化合物是共价化合物;
D.某元素原子最外层只有1个电子,它跟卤素可能形成离子键也可能形成共价键.
解答 解:A.含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,如铵盐等,故A正确;
B.两种不同的非金属元素形成的化合物中可能存在极性键和非极性键,如多C原子的烃等,故B错误;
C.只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,故C正确;
D.某元素原子最外层只有1个电子,它跟卤素可能形成离子键也可能形成共价键,如NaCl中存在离子键、HCl中存在共价键,故D正确;
故选B.
点评 本题考查化学键和化合物的关系,为高频考点,明确物质构成微粒是解本题关键,易错选项是D,注意采用举例法分析解答.

练习册系列答案
相关题目
7.80克Cu和Cu2O的混合物完全溶于适量的浓硝酸,共收集到31.36L气体(N0与NO2的混合气体),向收集到的气体中通人11.2L氧气恰好能完全溶于水(气体体积均换算成标准状况),则参加反应的硝酸的物质的量为( )
| A. | 1.4mol | B. | 2.4mol | C. | 3.8mol | D. | 5.2mol |
19.某工业废水中仅含下表离子中的5种(不考虑水的电离及离子的水解),且各种离子的物质的量浓度相等,均为0.1mol/L.
甲同学欲探究废水的组成,进行了如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量溶液于试管中,加入KSCN溶液后无明显变化.
Ⅲ.另取少量溶液于试管中,加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)甲同学最终确定原溶液中所含阴离子是Cl-、NO3-、SO42-(写离子符号).
(3)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+═3Fe3++NO+2H2O.
(4)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为1.6g.
(5)工业废水中常含有不同类型的污染物,可采用不同的方法处理.以下是乙同学针对含不同污染物的废水提出的处理措施和方法,其中正确的是D.
| 阳离子 | K+ Cu2+ Fe3+ Al3+ Fe2+ |
| 阴离子 | Cl- CO${\;}_{3}^{2-}$ NO${\;}_{3}^{-}$ SO${\;}_{4}^{2-}$ SiO${\;}_{3}^{2-}$ |
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,无紫色火焰(透过蓝色钴玻璃观察).
Ⅱ.取少量溶液于试管中,加入KSCN溶液后无明显变化.
Ⅲ.另取少量溶液于试管中,加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变.
Ⅳ.向Ⅲ中所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请推断:
(1)由Ⅰ、Ⅱ判断,溶液中一定不含有的阳离子是K+、Fe3+(写离子符号).
(2)甲同学最终确定原溶液中所含阴离子是Cl-、NO3-、SO42-(写离子符号).
(3)Ⅲ中加入少量盐酸生成无色气体的离子方程式是3Fe2++NO3-+4H+═3Fe3++NO+2H2O.
(4)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,得到的固体质量为1.6g.
(5)工业废水中常含有不同类型的污染物,可采用不同的方法处理.以下是乙同学针对含不同污染物的废水提出的处理措施和方法,其中正确的是D.
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含复杂有机物的废水 | 通过微生物代谢 | 物理法 |
| D | 碱性的废水 | 用CO2中和 | 化学法 |
17.a mol金属单质M和含2.5a mol HNO3的稀溶液恰好完全反应,氧化产物是M(NO3)2,则还原产物可能是( )
| A. | NO2 | B. | NO | C. | N2O5 | D. | NH4NO3 |
18.物质的量浓度相同的下列溶液中:①NH4Cl ②(NH4)2CO3 ③(NH4)2SO4 ④NH4HSO4⑤NH4HCO3 c(NH${\;}_{4}^{+}$)由大到小的顺序是( )
| A. | ⑤②③①④ | B. | ④①③②⑤ | C. | ③②①⑤④ | D. | ③②④①⑤ |
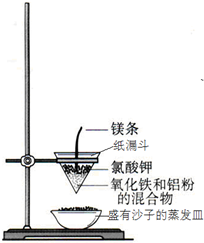 现代生活离不开铝,铝有许多优良的性能,因此在各方面有极其广泛的用途.
现代生活离不开铝,铝有许多优良的性能,因此在各方面有极其广泛的用途.