题目内容
18.物质的量浓度相同的下列溶液中:①NH4Cl ②(NH4)2CO3 ③(NH4)2SO4 ④NH4HSO4⑤NH4HCO3 c(NH${\;}_{4}^{+}$)由大到小的顺序是( )| A. | ⑤②③①④ | B. | ④①③②⑤ | C. | ③②①⑤④ | D. | ③②④①⑤ |
分析 ①NH4Cl ②(NH4)2CO3 ③(NH4)2SO4 ④NH4HSO4 ⑤NH4HCO3 ,先不考虑水解,则②(NH4)2CO3和③(NH4)2SO4都含有两个NH4+,所以它们NH4+的浓度大于其它三种物质,溶液中c(NH4+)根据盐类水解的影响分析判断.
解答 解:物质的量浓度相同的下列溶液:①NH4Cl、②(NH4)2CO3、③(NH4)2SO4、④NH4HSO4、⑤NH4HCO3;先不考虑水解,则②(NH4)2CO3 和 ③(NH4)2SO4 都含有两个NH4+,所以它们NH4+的浓度大于其它三种物质,而②(NH4)2CO3 中NH4+水解显酸性,CO32-水解显碱性,两者相互促进,所以NH4+水解的量较多,NH4+的量较少,③(NH4)2SO4中硫酸根离子对铵根离子浓度无影响,即溶液中c(NH4+)③>②;
①④⑤三种物质中,④NH4HSO4酸性最强,NH4+水解受到的抑制最大,即NH4+的量较多,溶液中c(NH4+)较大,
①NH4Cl,NH4+水解,④NH4HSO4,溶液中氢离子抑制铵根离子水解,即溶液中c(NH4+)④>①;
⑤NH4HCO3 ,HCO3- 水解促进铵根离子水解 溶液中c(NH4+)应最小,则①>⑤;
按c(NH4+)由大到小的顺序排列为:③>②>④>①>⑤,
故选:D.
点评 本题考查盐类水解的原理和应用,注意盐类水解的实质和把握弱电解质的电离,从影响平衡移动的角度分析离子浓度的大小比较是解答的关键,题目难度中等.

练习册系列答案
相关题目
8.下列说法不正确的是( )
| A. | 含有离子键的化合物一定是离子化合物 | |
| B. | 两种不同的非金属元素形成的化合物中只存在极性共价键 | |
| C. | 共价化合物不可能存在离子键 | |
| D. | 某元素原子最外层只有1个电子,它跟卤素可能形成离子键也可能形成共价键 |
9.为检验溶液里的某种离子,进行下列实验,其中结论正确的是( )
| A. | 溶液中加入稀HNO3后,再加AgNO3溶液有黄色沉淀生成,则溶液中一定含Br- | |
| B. | 溶液中加入BaCl2有白色沉淀,再加入稀硝酸沉淀不溶解,则溶液中一定含SO42- | |
| C. | 溶液中加入NaOH溶液,加热后能产生使湿润的红色石蕊试纸变蓝的气体,则溶液中一定含NH4+ | |
| D. | 进行某溶液的焰色反应时,观察火焰呈黄色,则溶液中一定不存在K+ |
3.实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:
4NH${\;}_{4}^{+}$+6HCHO═3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1mol H+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ称取样品1.500g.
步骤Ⅱ将样品溶解后,完全转移到250mL容量瓶中,定容、充分摇匀.
步骤Ⅲ移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数偏高(填“偏高”“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积无影响(填“偏大”“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察B.
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由无色变成浅红(或浅红)色.
(2)滴定结果如表所示:
若NaOH标准溶液的浓度为0.101 0mol•L-1,则该样品中氮的质量分数为18.85%.
4NH${\;}_{4}^{+}$+6HCHO═3H++6H2O+(CH2)6N4H+[滴定时,1mol(CH2)6N4H+与1mol H+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ称取样品1.500g.
步骤Ⅱ将样品溶解后,完全转移到250mL容量瓶中,定容、充分摇匀.
步骤Ⅲ移取25.00mL样品溶液于250mL锥形瓶中,加入10mL 20%的中性甲醛溶液,摇匀、静置5min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点.按上述操作方法再重复2次.
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数偏高(填“偏高”“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积无影响(填“偏大”“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察B.
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由无色变成浅红(或浅红)色.
(2)滴定结果如表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
10.化学中图象可以直观地描述化学反应的进程或结果,如图图象描述正确的是( )
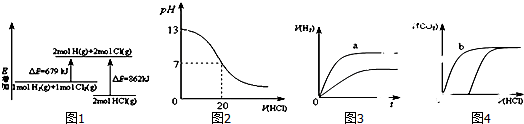

| A. | 图1表示化学反应H2(g)+Cl2(g)=2HCl(g)的能量变化,则该反应的反应热△H=183kJ•mol-1 | |
| B. | 图2表示室温时用0.1mol•L-1盐酸滴定10mL0.1mol•L-1NaOH溶液,溶液pH随加入酸体积变化 | |
| C. | 图3表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | 图4表示10mL0.1mol/LNa2CO3和NaHCO3两种溶液中,分别滴加0.1mol/LHCl,产生CO2的体积随盐酸体积的变化,则b表示Na2CO3溶液 |
7.以下说法不正确的是( )
| A. | 物质所含元素化合价升高的反应叫氧化反应 | |
| B. | 在氧化还原反应中,失去电子的元素化合价升高 | |
| C. | 元素从化合态(化合物形式)变为游离态(单质形式),一定是被还原 | |
| D. | 失电子越多的物质,其还原性越强 |
8.T℃时,在3L的密闭容器中充入4mol光气(COCl2),发生反应COCl2(g)?CO(g)+Cl2(g),同时还发生反应2CO(g)?2C(s)+O2(g),当反应达到平衡时,测得CO(g)和C(s)的物质的量分别为2mol和1mol,则该温度下,CO(g)+Cl2(g)?COCl2(g)的平衡常数K为( )
| A. | $\frac{1}{9}$ | B. | 2 | C. | $\frac{1}{3}$ | D. | $\frac{1}{2}$ |
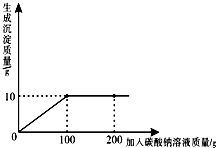 现有13.4g固体氯化钙样品(含杂质氯化钠),为了测定样品中氯化钙的含量,将此固体全部溶于96.6g水中,向所得的混合溶液中滴加一定质量分数的碳酸钠溶液,记录了如图所示的曲线关系.提示:氯化钙与碳酸钠反应的化学方程式:CaCl2+Na2CO3=CaCO3↓+2NaCl.
现有13.4g固体氯化钙样品(含杂质氯化钠),为了测定样品中氯化钙的含量,将此固体全部溶于96.6g水中,向所得的混合溶液中滴加一定质量分数的碳酸钠溶液,记录了如图所示的曲线关系.提示:氯化钙与碳酸钠反应的化学方程式:CaCl2+Na2CO3=CaCO3↓+2NaCl.