题目内容
(8分)(1)2 mol O3和3 mol O2的质量之比________,体积之比________.
(2)若12.4 g Na2X中含有0.4 mol钠离子,Na2X的摩尔质量是________ X的相对原子质量是________.
【答案】
(1)1∶1 2∶3
(2)62 g·mol-1 16
【解析】
试题分析:(1)O3和O2都是氧元素单质,质量比等于氧原子个数比,1∶1;根据阿伏伽德罗定律,气体体积比等于气体物质的量之比,2∶3。
(2) 12.4 g Na2X中含有0.4 mol钠离子,则Na2X为0.2mol,M(Na2X)= 12.4 g/0.2mol=62 g·mol-1 ;X的相对原子质量=62-46=16。
考点:本题考察阿伏伽德罗定律及有关物质的量的计算。

练习册系列答案
相关题目
(8分)(1)短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第___族。
|
|
|
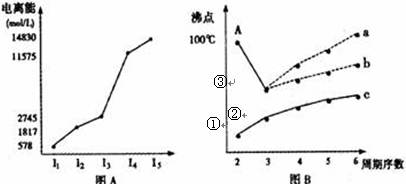 (2)图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律,①②③中表示为SiH4的是________
(2)图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律,①②③中表示为SiH4的是________
(3)不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线――折线a和折线b,你认为正确的是: ,理由是:_________________________________

(4)有三种固态物质,它们的性质如下:^S*5U.C#O%下
A物质:无色晶体,熔点3550℃,不导电,质硬,难溶于水及有机溶剂。
B物质:无色晶体,溶于水,质硬而脆,熔点800℃,熔化时能导电。
C物质:熔点-56.6℃,微溶于水,硬度小,固态或液态时不导电。
根据上述性质,可推断A和B的晶体类型为:A为________晶体,B为_________晶体。