题目内容
【题目】在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1L 0.1mol·L1 CH3COOH溶液中加入0.1mol CH3COONa固体,平衡后则溶液中![]() _______(填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度间的一个等式:_______________
_______(填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度间的一个等式:_______________
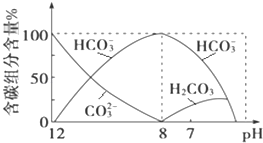
(2)常温下向20mL 0.1mol·L1 Na2CO3溶液中逐滴加入0.1mol·L1 HCl溶液40mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数随溶液pH变化的情况如下:
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32-________(填“能”或“不能”)大量共存;
②当pH=7时,溶液中含碳元素的主要微粒有__________、________,溶液中含量最多的三种微粒的物质的量浓度的大小关系为_________;
③已知在25℃时,CO32-水解反应的平衡常数Kh═2×104mol·L1,当溶液中c(HCO3-):c(CO32-)=2∶1时,溶液的pH=_____。
【答案】不变 c(CH3COO)+c(OH)=c(Na+)+c(H+) 不能 HCO H2CO3 c(Na+)>c(Cl)>c(HCO) 10
【解析】
(1)根据平衡常数表达式及溶液中电荷守恒原理分析解答;
(2)根据碳酸钠与盐酸的分步反应及图像中离子浓度大小分析解答;根据水解平衡常数及水的离子积计算溶液的pH。
(1)![]() 表示醋酸的电离平衡常数,只和温度有关,所以加入CH3COONa固体时保持不变,此时溶液中存在电荷守恒:c(CH3COO)+c(OH)=c(Na+)+c(H+),故答案为:不变;c(CH3COO)+c(OH)=c(Na+)+c(H+);
表示醋酸的电离平衡常数,只和温度有关,所以加入CH3COONa固体时保持不变,此时溶液中存在电荷守恒:c(CH3COO)+c(OH)=c(Na+)+c(H+),故答案为:不变;c(CH3COO)+c(OH)=c(Na+)+c(H+);
(2)常温下在20mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液40mL,先反应生成碳酸氢钠,再与盐酸反应生成二氧化碳、水,
①由反应及图象可知,在同一溶液中,H2CO3、HCO3、CO32不能大量共存,故答案为:不能;
②由图象可知,pH=7时,c(OH)=c(H+),溶液中含碳元素的主要微粒为HCO3、H2CO3,由电荷守恒可知c(Na+)+c(H+)=c(Cl)+c(HCO3)+c(OH),则c(Na+)>c(Cl),因HCO3水解,则c(Na+)>c(Cl)>c(HCO3),故答案为:HCO3、H2CO3;c(Na+)>c(Cl)>c(HCO3);
③CO32-的水解常数![]() ,当溶液中c(HCO3-):c(CO32-)=2∶1时,c(OH)=104mol/L,由Kw可知,c(H+)=1010mol/L,所以pH=10,故答案为:10。
,当溶液中c(HCO3-):c(CO32-)=2∶1时,c(OH)=104mol/L,由Kw可知,c(H+)=1010mol/L,所以pH=10,故答案为:10。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案