题目内容
4.有X、Y两种元素,相对原子质量分别为56、16,化合价分别为+3和-2,则X和Y组成的化合物的相对分子质量为?( )| A. | 72 | B. | 88 | C. | 160 | D. | 200 |
分析 X、Y两种元素化合价分别为+3和-2,则X、Y组成的化合物的化学式为:X2Y3;该物质的相对分子质量X和Y的相对原子质量之和.
解答 解:X、Y两种元素化合价分别为+3和-2,则X、Y组成的化合物的化学式为:X2Y3;X、Y两种元素的相对原子质量分别为56、16,其相对分子质量为56×2+16×3=160.
故选C.
点评 本题考查化合物的相对分子质量,准确写出化合物的化学式是解题的关键.

练习册系列答案
相关题目
14. 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )| A. | 2.7gAl与足量的该硫酸反应可得到标准状况下的H2 3.36L | |
| B. | 该硫酸50 mL与足量的铜反应可得到标准状况下SO2 10.3 L | |
| C. | 配制200 mL 4.6 mol•L-1的稀硫酸需该硫酸50 mL | |
| D. | 该硫酸与等体积的水混合所得溶液的质量分数小于49% |
15.3个氨基酸失去2个H2O缩合成三肽化合物,现有分子式为C36H57O18N11的十一肽化合物完全水解生成甘氨酸(C2H5O2N)、丙氨酸(C3H7O2N)、谷氨酸(C5H9O4N),在缩合成十一肽化合物时,这三种氨基酸的物质的量之比为( )
| A. | 3:3:5 | B. | 3:5:3 | C. | 5:3:3 | D. | 8:7:7 |
12.如图是部分短周期元素原子半径与原子序数的关系图.则下列说法正确的是( )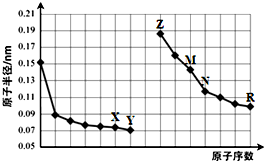

| A. | X、R两种元素的气态氢化物的稳定性:R>X | |
| B. | 简单离子的半径:Y>Z>M | |
| C. | N的单质能与Z的最高价氧化物对应的水化物反应 | |
| D. | Z与X两种元素形成的化合物都是碱性氧化物 |
19.已知标准状况下11.2LA气体分子的质量为16g,则A气体的摩尔质量是( )
| A. | 16g | B. | 32g | C. | 64g/mol | D. | 32g/mol |
9.碱金属和卤素形成的化合物大多具有的性质是( )
①较高沸点
②能溶于水
③水溶液能导电
④熔点很低
⑤熔融状态不导电.
①较高沸点
②能溶于水
③水溶液能导电
④熔点很低
⑤熔融状态不导电.
| A. | ①②③ | B. | ③④⑤ | C. | ①④⑤ | D. | ②③⑤ |
16.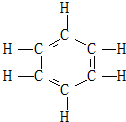 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构(如图),解释了苯的部分性质,但还有一些问题尚未解决,如它不能解释( )
1866年凯库勒提出了苯的单、双键交替的正六边形平面结构(如图),解释了苯的部分性质,但还有一些问题尚未解决,如它不能解释( )
①苯不能使溴的CCl4溶液褪色;②苯能与H2发生加成反应
③溴苯没有同分异构体 ④邻二溴苯只有一种.
 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构(如图),解释了苯的部分性质,但还有一些问题尚未解决,如它不能解释( )
1866年凯库勒提出了苯的单、双键交替的正六边形平面结构(如图),解释了苯的部分性质,但还有一些问题尚未解决,如它不能解释( )①苯不能使溴的CCl4溶液褪色;②苯能与H2发生加成反应
③溴苯没有同分异构体 ④邻二溴苯只有一种.
| A. | ①④ | B. | ④ | C. | ②③ | D. | ② |
13.下列离子方程式书写正确的是( )
| A. | 硅酸钠溶液中逐滴加入盐酸:Na2SiO3+2H+=H2SiO3↓+2Na2+ | |
| B. | 向氢氧化钠溶液中加入醋酸溶液:OH-+H+=H2O | |
| C. | 铜与稀硝酸反应:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| D. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
14.将锌片和铜片用导线连接置于同一稀硫酸中组成原电池,下列叙述不正确的是( )
| A. | 锌片发生氧化反应 | B. | 铜片发生还原反应 | ||
| C. | 铜片上有氢气析出 | D. | 电子从锌片流出,流向铜片 |