题目内容
下列表示对应化学反应的离子方程式正确的是
| A.足量Cl2通入FeBr2溶液中:Br-+ Cl2 = Br2 +2Cl- |
| B.用NaClO除去水体中CO(NH2)2产生CO2和N2:3ClO +CO(NH2)2=3Cl- +CO2↑+N2↑+2H2O |
| C.过量CO2通入Na2SiO3溶液中:Si032-+CO2+H2O = H2SiO3↓+CO32- |
| D.Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2+ +HCO3-+OH-= CaCO3↓+H2O |
B
解析试题分析:A、Cl2足量,Fe2+和Br-均要被氧化,错误;B、ClO-氧化CO(NH2)2,Cl从+1降到-1,N从-3降到0价,依据得失电子守恒可配平反应,正确;C、CO2过量,应生成HCO3- ,错误;D、Ca(HCO3)2少量,则Ca2+与HCO3- 应满足1:2的关系,错误。
考点:离子方程式的书写及正误判断

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
下列离子或物质组能大量共存,且满足相应条件的是
| 选项 | 离子或物质 | 条件 |
| A | Na+、K+、Cl-、SO42- | c(Na+)+c(K+)=c(SO42-)+ c(Cl-) |
| B | Fe3+、SO32-、Cl- | 加入NaOH溶液,产生红褐色沉淀 |
| C | Ba+、HCO3-、Cl-、H+ | 加入氨水产生沉淀 |
| D | SO2、O2、NO2 | 通入足量NaOH溶液后,可能会没有任何气体剩余 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.01 mol·L-1Ba(OH)2溶液:Al3+、NH4+、NO3-、HCO3- |
| B.加入甲基橙显红色的溶液:Mg2+、Fe2+、Cl-、NO3- |
| C.含有苯酚的溶液中:K+、NH4+、Br-、Fe3+ |
| D.0.01mol·L-1HCl溶液:K+、Na+、I-、SO42- |
下列反应的离子方程式正确的是
A.NH4HCO3溶液与过量NaOH溶液共热:NH4++ OH一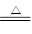 NH3↑+H2O NH3↑+H2O |
| B.Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ |
| C.向海带灰浸出液中加入稀硫酸、双氧水:2I-+2H++H2O2=I2+2H2O |
| D.Ba(OH)2溶液中滴加NaHSO4溶液至中性:Ba2++OH-+H++SO42一=BaSO4↓ +H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0.1 mol·L-1 KNO3溶液:Mg2+、Fe2+、Cl-、SO42- |
| B.无色透明的溶液:Cu2+、NH4+、NO3-、CO32- |
| C.使pH试纸变红的溶液:K+、Ca2+、Cl-、ClO- |
| D.水电离出的c(H+)=10-12 mol·L-1的溶液:Na+、NH4+、SO42-、NO3- |
在水溶液中能大量共存的一组是
| A.NH4+、Ag+、CO32-、SO42- | B.Fe2+、H+、MnO4-、HCO3- |
| C.K+、Na+、NO3-、SO42- | D.Al3+、Mg2+、C1-、SiO32- |
在水溶液中能大量共存的一组离子是
| A.NH4+、Na+、Br¯、SO42¯ | B.Fe2+、H+、ClO¯、Cl¯ |
| C.K+、Ca2+、OH¯、NO3¯ | D.Mg2+、H+、SiO32¯、SO42¯ |
能在水溶液中大量共存的一组离子是
| A.Na+、Mg2+、I-、ClO- | B.Al3+、NH4+、SO42-、Cl- |
| C.K+、Ag+、NO3-、Cl- | D.NH4+、Na+、OH-、SiO32- |
下列离子方程式中,正确的
| A.在AlCl3溶液中加入过量氨水:Al3+ + 3NH3·H2O =Al(OH)3↓ + 3NH4+ |
| B.大理石加入过量盐酸中:CO32-+2H+= CO2↑+H2O |
| C.稀硫酸和Ba(OH)2溶液反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D.在CuSO4溶液中加入Ba(OH)2溶液:Ba2+ + SO42- =BaSO4↓ |