题目内容
14.设NA为阿伏加德罗常数的值.下列说法正确的是( )| A. | 0.1 mol Cl2参加反应,转移的电子数目一定为0.2NA | |
| B. | 1.4g聚乙烯中含C-H数目为0.2NA | |
| C. | 标准状况下,5.6L甲醇中含有的分子数目为0.2NA | |
| D. | 常温下,pH=13的NaOH溶液中含OH-的数目为0.1NAA |
分析 A、根据反应后氯元素的价态来分析;
B、聚乙烯的最简式为CH2;
C、标况下,甲醇为液态;
D、溶液体积不明确.
解答 解:A、由于反应后氯元素的价态可能为-1价或+1价或+3价或+5价或+7价,故0.1mol氯气参与反应转移的电子不一定为0.2NA个,故A错误;
B、聚乙烯的最简式为CH2,故1.4g聚乙烯中含有的CH2的物质的量n=$\frac{14g}{14g/mol}$=0.1mol,则含0.2molC-H键即0.2NA个,故B正确;
C、标况下,甲醇为液态,不能根据气体摩尔体积来计算其物质的量,故C错误;
D、溶液体积不明确,故溶液中氢氧根的个数无法计算,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.在一定温度时,将1mol A和2mol B放入容积为5L的某密闭容器中发生如下反应:A(s)+2B(g)?C(g)+2D(g),经5min后测得容器内B的浓度减少了0.2mol•L-1.下列叙述不正确的是( )
| A. | 在5 min内该反应用C表示的反应速率为0.02 mol•L-1•min-1 | |
| B. | 5 min时,容器内D的浓度为0.2 mol•L-1 | |
| C. | 当容器内压强保持恒定时,该可逆反应达到平衡状态 | |
| D. | 5 min时容器内气体总的物质的量为3 mol |
2.下列现象或事实可用同一化学原理加以说明的是( )
| A. | 氯化铵和碘都可以用加热法进行提纯 | |
| B. | 铜和氯化钠溶液均能导电 | |
| C. | 硫酸亚铁溶液和氢氧化钠溶液在空气中留置均会变质 | |
| D. | 铁片和铝片置于冷的浓硫酸中均无明显现象 |
9.下列反应的离子方程式正确的是( )
| A. | 澄清石灰水中滴加少量的小苏打溶液:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 铵明矾[NH4Al(SO4)2•12H2O]溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O | |
| C. | 过氧化钠和水反应:2O22-+2H2O═4OH-+O2↑ | |
| D. | H2O2溶液中滴加酸性KMnO4溶液:2MnO4-+5 H2O2+6H+═2Mn2++5O2↑+8H2O |
19.岩白菜素具有镇痛、镇静及安定作用等作用,其结构简式如图,下列说法正确的是( )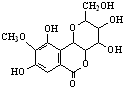

| A. | 能与FeCl3溶液发生显色反应 | |
| B. | 该分子中含有3个手性碳原子 | |
| C. | 该化合物可与Br2发生取代反应 | |
| D. | 1mol该化合物最多可与5molNaOH反应 |
6.某反应进行过程中,各物质物质的量的变化情况如图所示.下列说法正确的是( )


| A. | C、D是生成物 | B. | 反应的方程式为:2A+B═2C | ||
| C. | 2min后各物质的量不再变化 | D. | 该反应不是可逆反应 |
4.下列叙述正确的是( )
| A. | NaCl、MgCl2等物质熔融状态时都导电,因此它们都是电解质 | |
| B. | HCl、H2SO4液态时都不导电,因此它们都是非电解质 | |
| C. | 易溶于水的化合物都是电解质 | |
| D. | 浓溶液的导电能力一定强 |