题目内容
4.苯硫酚(PhSH)是一种用途广泛的有机合成中间体.工业上用常用氯苯(PhCl)和硫化氢(H2S)在高温下反应来制备苯硫酚,但会有副产物苯(PhH)生成.I:PhCl(g)+H2S(g)?PhSH(g)+HCl(g)△H1=-16.8kJ•mol-1
II:PhCl(g)+H2S(g)═PhH(g)+HCl(g)+$\frac{1}{8}$S8(g)△H2
回答下列问题:
(1)反应 I为可逆反应,写出平衡常数的表达式K=$\frac{c(PhSH)×c(HCl)}{c(PhCl)×c({H}_{2}S)}$,反应 II为不可逆反应,△H2=<0.(填写“>”,“<”,“=”)
(2)上述两个反应的能量变化如图一所示,则在某温度时反应速度v( I)> v( II).(填写“>”,“<”,“=”)
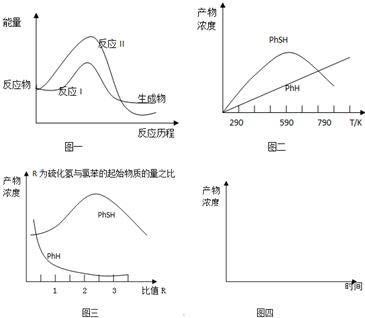
(3)现将一定量的氯苯和硫化氢置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20分钟测定生成物的浓度,得到图二和图三.
①请解释图二中两条曲线的变化开始时,反应Ⅰ速率大于反应Ⅱ速率,所以生成苯硫酚浓度大于苯;反应Ⅰ达到平衡后,温度升高,平衡逆向移动,所以生成物苯硫酚浓度减小;反应Ⅱ是不可逆反应,温度升高反应速率加快,生成的苯浓度增加,消耗了反应物,进一步导致反应Ⅰ逆向移动.
②若要提高主产物苯硫酚的产量,可采取的措施是R=2.5,温度控制在590K.
(4)请根据图二、图三,画出恒温恒容条件下反应主产物苯硫酚的物质的量随时间变化的曲线图.
分析 (1)化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比;由图1可知,Ⅱ中反应物总能量高于生成物总能量,反应Ⅱ为放热反应;
(2)活化能越高,反应速率应越慢;
(3)①开始时,反应Ⅰ速率大于反应Ⅱ速率,所以生成苯硫酚浓度大于苯;反应Ⅰ达到平衡后,温度升高,平衡逆向移动,所以生成物苯硫酚浓度减小;反应Ⅱ是不可逆反应,温度升高反应速率加快,生成的苯浓度增加,消耗了反应物,进一步导致反应Ⅰ逆向移动;
②由图三可知,R=2.5时PhSH浓度最大,由图二可知,温度590K时PhSH浓度最大;
(4)恒温恒容条件下,苯硫酚的物质的量随反应进行浓度增大,到达平衡后浓度最大,而平衡后苯浓度增加,消耗了反应物,导致反应Ⅰ逆向移动,苯硫酚的物质的量减小.
解答 解:(1)化学平衡常数为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比,反应Ⅰ的平衡常数的表达式K=$\frac{c(PhSH)×c(HCl)}{c(PhCl)×c({H}_{2}S)}$;由图1可知,Ⅱ中反应物总能量高于生成物总能量,反应Ⅱ为放热反应,故△H<0,
故答案为:$\frac{c(PhSH)×c(HCl)}{c(PhCl)×c({H}_{2}S)}$;<;
(2)活化能Ⅱ>I,活化能越高,单位体积内活化分子数目越小,反应速率应越慢,故反应速率v(Ⅰ)>v(Ⅱ),
故答案为:>;
(3)①开始时,反应Ⅰ速率大于反应Ⅱ速率,所以生成苯硫酚浓度大于苯;反应Ⅰ达到平衡后,温度升高,平衡逆向移动,所以生成物苯硫酚浓度减小;反应Ⅱ是不可逆反应,温度升高反应速率加快,生成的苯浓度增加,消耗了反应物,进一步导致反应Ⅰ逆向移动,PhSH的浓度又降低,
故答案为:开始时,反应Ⅰ速率大于反应Ⅱ速率,所以生成苯硫酚浓度大于苯;反应Ⅰ达到平衡后,温度升高,平衡逆向移动,所以生成物苯硫酚浓度减小;反应Ⅱ是不可逆反应,温度升高反应速率加快,生成的苯浓度增加,消耗了反应物,进一步导致反应Ⅰ逆向移动;
②由图三可知,R=2.5时PhSH浓度最大,由图二可知,温度590K时PhSH浓度最大,故采取措施为:,
故答案为:R=2.5,温度控制在590K;
(4)恒温恒容条件下,苯硫酚的物质的量随反应进行浓度增大,到达平衡后浓度大最大,而平衡后苯浓度增加,消耗了反应物,导致反应Ⅰ逆向移动,苯硫酚的物质的量减小,苯硫酚的物质的量随时间变化的曲线图为: ,
,
故答案为: .
.
点评 本题考查化学反应速率及化学平衡图象综合应用、平衡常数、化学反应能量变化等,是对学生综合能力的考查,难度中等.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案| A. | 氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾 | |
| B. | 铜在氯气中燃烧,产生棕黄色烟,产物溶于水,溶液呈蓝绿色 | |
| C. | 铁丝在氯气中燃烧,产生红色的浓烟,产物溶于水,溶液呈浅绿色 | |
| D. | 钠在空气中燃烧,发出黄色的火焰,生成白色固体 |
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 | 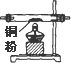 |  |  |  |  |  |
(1)如果所制得气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)
③接⑤接④接②接①接⑥;其中,②与④装置相连时,玻璃管接口(用装置中字母表示)应是接C.
(2)装置⑥中发生反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O.
(3)实验开始时,应首先检验装置的气密性;实验结束时,应先熄灭①处的酒精灯.
(4)在装置⑤的烧瓶中,发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2+2H2O
(5)待充分反应后,装置①的玻璃管中呈棕黄色.冷却后,将制得的产物配成溶液,溶液呈绿(或蓝绿)色.
(6)若反应中有71gCl2生成,则被氧化的HCl的物质的量为2mol,转移电子数为2NA.
| A. | 同物质的量浓度的三种溶液的pH:a>b>c | |
| B. | 同pH时,三种溶液稀释相同倍数后,pH:a>b<c | |
| C. | 同pH、同体积的三种溶液消耗同浓度盐酸 的体积:a=b=c | |
| D. | 同pH时,稀释不同倍数、pH仍相同,三种溶液稀释的倍数:a>b>c |
| A. | 1:3.4 | B. | 1:1.7 | C. | 2.6:1 | D. | 4.6:1 |
| A. | 0.1 mol Cl2参加反应,转移的电子数目一定为0.2NA | |
| B. | 1.4g聚乙烯中含C-H数目为0.2NA | |
| C. | 标准状况下,5.6L甲醇中含有的分子数目为0.2NA | |
| D. | 常温下,pH=13的NaOH溶液中含OH-的数目为0.1NAA |

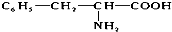 )相同,且同时符合下列两个条件:①苯环上带有两个取代基,②有一个硝基直接连在苯环上,则符合此条件的同分异构体数目是( )
)相同,且同时符合下列两个条件:①苯环上带有两个取代基,②有一个硝基直接连在苯环上,则符合此条件的同分异构体数目是( )