题目内容
11.燃烧电池的制作(1)把两根碳棒放在酒精喷灯上灼烧2-3min,立即投入到冷水中,反复操作3-5次,其主要目的是使碳棒表面变得粗糙多孔,即制得多孔碳电极.

(2)如图装置,两玻璃管中盛满KNO3溶液,C(Ⅰ),C(Ⅱ)为上述处理过的碳棒(多孔石墨电极).
①接通S1后,两玻璃管中有气体生成,其电解的反应式为2H2O$\frac{\underline{\;电解\;}}{\;}$O2↑+2H2↑.
②电解一段时间后,当两玻璃管中液面未脱离电极,多孔石墨电极上有吸附着许多小气泡时,断开S1,接通S2,电流表的指针发生偏转,电子流动方向如图所示.此时:
C(Ⅰ)的电极名称是负极,电极反应式为2H2-4e-═4H+.
C(Ⅱ)的电极名称是正极,电极反应式为O2+4e-+2H2O═4OH-.
分析 (1)碳棒放在酒精喷灯上灼烧2-3min,立即投入到冷水中,反复操作3-5次主要是使碳棒表面变得粗糙多孔,即制得多孔碳电极;
(2)①解KNO3溶液时,实质为电解水,阳极上氢氧根离子放电生成氧气,阴极上氢离子放电生成氢气;
②根据①的分析,一端生成氧气,一端生成氢气,断开S1,接通S2,形成原电池,电流表的指针发生偏转,根据电子流动方向,所以C(I)为负极,负极应为氢气发生氧化反应,C(Ⅱ)为正极,正极应为氧气发生还原反应,据此分析.
解答 解:(1)(1)碳棒放在酒精喷灯上灼烧2-3min,立即投入到冷水中,反复操作3-5次主要是使碳棒表面变得粗糙多孔,即制得多孔碳电极,
故答案为:使碳棒表面变得粗糙多孔,即制得多孔碳电极;
(2)①电解KNO3溶液时,实质为电解水,阳极上氢氧根离子放电生成氧气气,阴极上氢离子放电生成氢气,则电池反应式为:2H2O$\frac{\underline{\;电解\;}}{\;}$O2↑+2H2↑,
故答案为:2H2O$\frac{\underline{\;电解\;}}{\;}$O2↑+2H2↑;
②根据①的分析,一端生成氧气,一端生成氢气,断开S1,接通S2,形成原电池,电流表的指针发生偏转,根据电子流动方向,所以C(I)为负极,负极应为氢气发生氧化反应,电极反应式为:2H2-4e-═4H+;C(Ⅱ)为正极,正极应为氧气发生还原反应,电极反应式为:O2+4e-+2H2O═4OH-;
故答案为:负极;2H2-4e-═4H+;正极;O2+4e-+2H2O═4OH-.
点评 本题考查了电解池和原电池的有关知识,涉及到电极反应式的书写和总反应的书写等,题目难度不大,注意把握电解池和原电池的工作原理.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.据报道,碳纳米管是碳原子形成的大分子,其导电性是铜的1万倍;N5可用作烈性炸药.下列说法正确的是( )
| A. | 金刚石与碳纳米管互为同分异构体 | B. | N3与N2互为同素异形体 | ||
| C. | 14C的质量数为14 | D. | C原子半径比N原子半径小 |
6.NA代表阿伏伽德罗常数的值,已知C2H4和C3H6的混合物的质量为ag,则该混合物( )
| A. | 所含共用电子对数为($\frac{a}{7}+1$)NA | B. | 所含碳氢键数目为$\frac{a{N}_{A}}{7}$ | ||
| C. | 燃烧时消耗的O2一定是$\frac{33.6a}{14}$L | D. | 所含原子总数为$\frac{a{N}_{A}}{14}$ |
16.石墨和金刚石都是碳的单质,石墨在一定条件下可转化为金刚石.已知12g石墨完全转化为金刚石时,要吸收E kJ的能量,下列说法正确的是( )
| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石和石墨互为同位素 | |
| C. | 石墨能量高于金刚石 | |
| D. | 等质量的金刚石与石墨完全燃烧,石墨放出的能量少 |
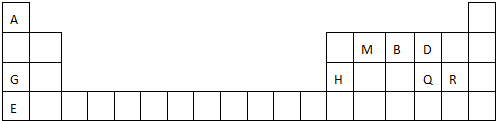
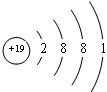
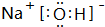 ; 用电子式表示G与Q形成化合物的过程
; 用电子式表示G与Q形成化合物的过程 ;
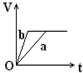
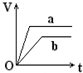
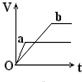
;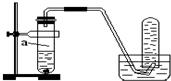 向足量的a、b两份锌粉中,分别加入少量且等量的稀H2SO4,同时向a中加入少量的CuSO4溶液.下图表示产生H2的体积(V)与时间(t)的关系,其中正确的是( )
向足量的a、b两份锌粉中,分别加入少量且等量的稀H2SO4,同时向a中加入少量的CuSO4溶液.下图表示产生H2的体积(V)与时间(t)的关系,其中正确的是( )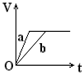

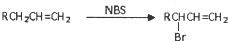
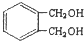 的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式
的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式 (其中之一).
(其中之一).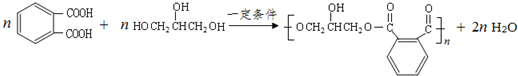 .
.