题目内容
12.设计燃料电池使汽油氧化直接产生电流,是重要的课题之一.最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入汽油蒸气(以辛烷为汽油的代表物),电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-.下列说法正确的是( )| A. | 固体电解质里O2-的移动方向是由负极到正极 | |
| B. | 电池工作时电流由通汽油蒸汽的电极经外电路到通空气的电极 | |
| C. | 负极的电极反应式为C8H18+25O2--50e-═8CO2+9H2O | |
| D. | 正极的电极反应式为O2+2H2O+4e-═4OH- |
分析 燃料电池的总反应和燃料燃烧的化学方程式一致,正极是氧气发生得电子的还原反应,总反应减正极反应可得负极反应式;原电池工作时,阴离子向负极移动,电子从负极经外电路流向正极,电流从正极流向负极,据此回答.
解答 解:A、原电池中,固体电解质里O2-的移动方向是由正极到负极,故A错误;
B、电池工作时,通空气的电极是正极,通入燃料的电极是负极,电流由通空气的电极到通汽油蒸汽的电极,故B错误;
C、燃料电池的负极上是燃料发生失电子的氧化反应,即C8H18+25O2--50e-═8CO2+9H2O,故C正确;
D、总反应减负极反应可得正极反应式,正极的电极反应式为O2+4e-=2O2-,故D错误.
故选C.
点评 本题考查化学电源新型电池以及原电池的工作原理知识,题目难度中等,注意电极反应式的书写是关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.某烃的结构简式为 ,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a,b,c分别为( )
,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a,b,c分别为( )
 ,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a,b,c分别为( )
,分子中含有四面体结构的碳原子数为a,在同一直线上的碳原子数最多为b,一定在同一平面内的碳原子数为c,则a,b,c分别为( )| A. | 4,3,5 | B. | 5,3,6 | C. | 2,5,4 | D. | 4,6,4 |
3.对于反应4NH3+5O2═4NO+6H2O,下列为四种不同情况下测得的反应速率,其中能表明该反应进行最快的是( )
| A. | v (NH3)=0.25 mol/(L•s) | B. | v (O2)=1.4mol/(L•min) | ||
| C. | v (H2O)=0.25 mol/(L•s) | D. | v (NO)=9 mol/(L•min) |
20.下列关于实验原理或操作的叙述中,正确的是( )
| A. | 在铜锌原电池中,往电解质溶液(稀硫酸)中加入重铬酸钾或双氧水能使电池放电时间缩短 | |
| B. | 溶液的酸碱性、催化剂都对H2O2的稳定性有很大影响,新鲜的动物肝脏能加快H2O2的分解 | |
| C. | 在镀锌铁皮锌镀层厚度测定实验中,当铁皮在盐酸中充分反应至速率突然减小时,应立即将铁片取出,用酒精喷灯烘干 | |
| D. | 在食醋总酸含量测定中,用已知浓度的氢氧化钠溶液滴定,以甲基橙作为指示剂滴定至终点 |
7.关于有机物的以下说法中,不正确的是( )
| A. | 油脂的氢化属于还原反应,又属于加成反应,生成物为纯净物 | |
| B. | 油酸既能够使Br2的四氯化碳溶液褪色,也可使酸性KMnO4溶液褪色 | |
| C. | 蔗糖、麦芽糖的化学式都可表示为C12H22O11,二者互为同分异构体 | |
| D. | 向鸡蛋白溶液中加入饱和硫酸铵溶液析出白色沉淀,不属于化学变化 |
4.下列说法不正确的是( )
| A. | 由分子组成的物质中一定存在共价键 | |
| B. | 全部由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 相同非金属原子间形成的化学键只存在于双原子单质分子中 | |
| D. | 同种原子间不可能形成离子键 |
1.已知甲和乙的某些性质如下表所示
据此,将甲和乙组成的混合物分离的最佳操作是( )
| 物质 | 熔点 | 沸点 | 密度 | 水中溶解性 |
| 甲 | -98℃ | 57.7℃ | 0.93g/cm3 | 可溶 |
| 乙 | -84℃ | 87℃ | 0.90g/cm3 | 可溶 |
| A. | 萃取 | B. | 过滤 | C. | 蒸馏 | D. | 分液 |
2.下列有关实验操作正确的是( )
| A. | 用100mL量筒量取2.25mL NaOH溶液 | |
| B. | 取用固体药品时一定要用镊子 | |
| C. | 由于NaOH有较强的腐蚀性,且能和玻璃中成分SiO2反应,因此称量NaOH固体时,不能用玻璃器皿只能用滤纸放在托盘天平上 | |
| D. | 实验室收集NO时只能用排水集气法,收集NO2时只能用排空气集气法 |
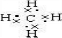 写出氨气的结构式
写出氨气的结构式