题目内容
20.下列关于实验原理或操作的叙述中,正确的是( )| A. | 在铜锌原电池中,往电解质溶液(稀硫酸)中加入重铬酸钾或双氧水能使电池放电时间缩短 | |
| B. | 溶液的酸碱性、催化剂都对H2O2的稳定性有很大影响,新鲜的动物肝脏能加快H2O2的分解 | |
| C. | 在镀锌铁皮锌镀层厚度测定实验中,当铁皮在盐酸中充分反应至速率突然减小时,应立即将铁片取出,用酒精喷灯烘干 | |
| D. | 在食醋总酸含量测定中,用已知浓度的氢氧化钠溶液滴定,以甲基橙作为指示剂滴定至终点 |
分析 A.在原电池反应中加入强氧化剂,它可以使Zn电极部分形成一层氧化膜,从而大大改善Zn电极金属的溶解速率,使电极的极化作用得以减缓;
B.新鲜的动物肝脏对双氧水的分解具有明显效果,分解速率受外界因素的影响;
C.酒精灯烘干,铁易被氧化;
D.以甲基橙作为指示剂,滴定终点与反应终点差距大,导致误差较大.
解答 解:A.在原电池反应中加入强氧化剂,它可以使Zn电极部分形成一层氧化膜,从而大大改善Zn电极金属的溶解速率,使电极的极化作用得以减缓,则往电解质溶液(稀硫酸)中加入重铬酸钾或双氧水能使电池放电时间延长,故A错误;
B.双氧水的分解速率受外界因素的影响,溶液的酸碱性、催化剂、新鲜的动物肝脏都对H2O2的稳定性有很大影响,新鲜的动物肝脏能加快H2O2的分解,故B正确;
C.当锌镀层完全反应后就是铁与盐酸反应,由于锌和铁的活泼性不同,反应速率就不同,待产生的气泡明显减少时取出,洗涤,烘干,称重,测出反应前后铁皮的质量,故C错误;
D.在食醋总酸含量测定中,用已知浓度的氢氧化钠溶液滴定,以酚酞作为指示剂滴定至终点,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及原电池、反应速率、电镀及中和滴定实验等,把握物质的性质、实验技能为解答的关键,侧重分析与实验能力的考查,题目难度较大.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目
10.能说明苯分子苯环的平面正六边形结构中,碳碳键不是单双键交替排布的事实是( )
| A. | 苯不能使溴水褪色 | B. | 苯能与H2发生加成反应 | ||
| C. | 苯的邻位二元取代物只有一种 | D. | 苯的对位二元取代物只有一种 |
11.化学与人类生活、社会可持续发展密切相关,下列说法正确的是( )
| A. | “天宫一号”中使用的碳纤维,是一种纤维素 | |
| B. | 回收制革工厂的边角皮料生产食用明胶,加工成医用胶囊或做食品增稠剂 | |
| C. | 氯化汞(HgCl2)的稀溶液可用于手术器械消毒,因为它会使蛋白质变性,杀菌消毒 | |
| D. | 蛋白质、淀粉、纤维素、油脂、葡萄糖等都能在人体内水解并提供能量 |
8.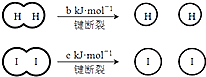 H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )
H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )
 H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )
H2和I2在一定条件下能发生反应:H2(g)+I2(g)?2HI(g)△H=-akJ•mol-1已知:(a、b、c均大于零),下列说法不正确的是( )| A. | 反应物的总能量高于生成物的总能量 | |
| B. | 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 | |
| C. | 断开2 mol H-I键所需能量约为(c+b+a)kJ | |
| D. | 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
5.如图为铜锌原电池示意图,下列说法正确的是( )
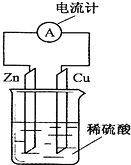

| A. | 锌片上有气泡产生 | B. | 烧杯中溶液逐渐呈蓝色 | ||
| C. | 电流由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
12.设计燃料电池使汽油氧化直接产生电流,是重要的课题之一.最近有人制造了一种燃料电池,一个电极通入空气,另一个电极通入汽油蒸气(以辛烷为汽油的代表物),电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-.下列说法正确的是( )
| A. | 固体电解质里O2-的移动方向是由负极到正极 | |
| B. | 电池工作时电流由通汽油蒸汽的电极经外电路到通空气的电极 | |
| C. | 负极的电极反应式为C8H18+25O2--50e-═8CO2+9H2O | |
| D. | 正极的电极反应式为O2+2H2O+4e-═4OH- |
9.高硬度的水对生活和生产都有危害,常需软化处理以降低硬度.下列方法不能降低硬度的是( )
| A. | 过滤 | B. | 离子交换法 | C. | 蒸馏 | D. | 加入软化药剂 |
10.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 78g Na2O2与足量水反应中电子转移了2NA | |
| B. | 只有在标准状况下NA个氧气分子的物质的量才是1mol | |
| C. | 常温常压下,28g N2气体的分子数小于NA | |
| D. | 标准状况下,1mol C5H12所含的共价键为16NA |
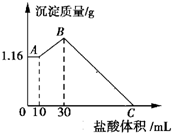 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,有1.16g 白色沉淀生成,再向所得的悬浊液中逐滴加入1mol•L-1 盐酸,加入盐酸的体积V与生成沉淀的质量关系如图所示.试回答下列问题:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,有1.16g 白色沉淀生成,再向所得的悬浊液中逐滴加入1mol•L-1 盐酸,加入盐酸的体积V与生成沉淀的质量关系如图所示.试回答下列问题: