题目内容
【题目】乙二酸(H2C2O4)俗称草酸,在实验研究和化学工业中应用广泛。草酸溶液中各粒子的物质的量分数随溶液pH变化关系如下图,下列说法正确的是
已知:①室温下,0.1 mol· L-1 H2C2O4的pH=1.3 ;0.1 mol· L-1NaHC2O4的pH=2.8
②草酸钙(Ca C2O4)难溶于水;
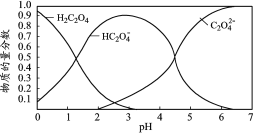
A.pH=4.5的草酸溶液中含有的大量微粒有:H2C2O4、HC2O4-、C2O42-
B.0.1 mol·L1 NaHC2O4溶液中:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4)
C.向H2C2O4溶液中加入酸性高锰酸钾溶液,紫色褪去:2MnO4-+5C2O42-+16H+=2Mn2+ +10CO2↑ +8H2O
D.向NaHC2O4溶液中加入足量澄清石灰水,产生白色沉淀:2HC2O4- +Ca2++2OH-=Ca C2O4↓ +2H2O+C2O42-
【答案】B
【解析】
A. pH=4.5的草酸溶液中含有的大量微粒有:HC2O4-、C2O42-,A错误;
B. NaHC2O4是强碱弱酸盐,产生Na+、HC2O4-,HC2O4-既发生电离作用产生C2O42-和H+,也发生水解作用产生H2C2O4、OH-,0.1 mol·L1 NaHC2O4溶液pH=2.8,说明其电离作用大于水解作用,所以c(C2O42-)>c(H2C2O4),电离、水解消耗HC2O4-,则c(Na+)>c(HC2O4-),但主要以盐电离产生的离子形式存在,c(HC2O4-)>c(C2O42-)>c(H2C2O4),故溶液中各种微粒浓度大小关系为:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4),B正确;
C. 草酸是二元弱酸,主要以酸分子存在,应该写化学式,C错误;
D. 向NaHC2O4溶液中加入足量澄清石灰水,溶液中含有大量Ca2+,反应产生草酸钙白色沉淀,不可能还存在C2O42-,D错误;
故合理选项是B。

 阅读快车系列答案
阅读快车系列答案