题目内容
【题目】FeCl3在现代工业生产中应用广泛。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。工业上,向500—600℃的铁屑中通入氯气可生产无水氯化铁;向炽热铁屑中通入氯化氢可以生产无水氯化亚铁。
某化学研究性学习小组模拟工业生产流程制备无水FeCl3并对产物做了如下探究实验,
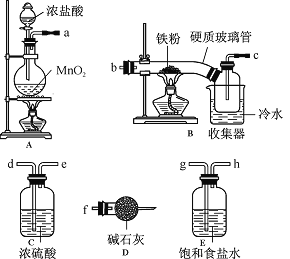
请回答下列问题:
(1)装置的连接顺序为 (用a、b、c…h表示)。
(2)i.E中饱和食盐水的作用是 。
ii.D中碱石灰的作用是 。
(3)反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端。要使沉积得FeCl3进入收集器,需进行的操作是 。
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
![]()
①淡黄色溶液中加入试剂X生成淡红色溶液的离子方程式为
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是 (用离子方程式表示)。
(5)已知红色褪去的同时有气体生成,经检验为O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同物质的量浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
实验①说明 ;
实验②的目的是 ;
得出结论: 。
【答案】(1)aghdebcf;
(2)i.除去氯气中的氯化氢气体,防止生成FeCl2杂质;防止H2和Cl2混合爆炸;
ii.吸收没有反应完的氯气,以防污染空气;吸收空气中的水蒸气,防止生成的FeCl3潮解
(3)在沉积的FeCl3固体下方加热;
(4)①Fe3++3SCN-![]() Fe(SCN)3;②2Fe2+ + 2H+ + H2O2 =2Fe3+ + 2H2O
Fe(SCN)3;②2Fe2+ + 2H+ + H2O2 =2Fe3+ + 2H2O
(5)实验①说明SCN-发生了反应而不是Fe3+发生反应;实验②的目的是排除H2O2分解产生的O2氧化SCN-的可能;结论:H2O2将SCN-氧化成SO42—
【解析】
试题分析:(1)浓硫酸具有吸水性能作氯气干燥剂、碱石灰具有碱性而吸收氯气、饱和食盐水吸收氯化氢而抑制氯气溶解,装置排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理,所以装置连接顺序为a→g→h→d→e→b→c→f,故答案为:a、g、h、d、e、b、c、f;
(2)i饱和食盐水吸收氯化氢而抑制氯气溶解,防止生成FeCl2杂质;同时可以防止H2和Cl2混合爆炸;故答案为:除去氯气中的氯化氢气体,防止生成FeCl2杂质;防止H2和Cl2混合爆炸;
ii. D中碱石灰可以吸收没有反应完的氯气,以防污染空气;吸收空气中的水蒸气,防止生成的FeCl3潮解,故答案为:吸收没有反应完的氯气,以防污染空气;吸收空气中的水蒸气,防止生成的FeCl3潮解;
(3)反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端。加热易升华,要使沉积得FeCl3进入收集器,在沉积的FeCl3固体下方加热,故答案为:在沉积的FeCl3固体下方加热;
(4)①Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈血红色,反应方程式为Fe3++3SCN-![]() Fe(SCN)3;②Fe2+被H2O2氧化生成Fe3+,从而增大Fe3+浓度,Fe3+、SCN-反应生成Fe(SCN)3,从而增大络合物浓度,溶液颜色加深,离子方程式为2Fe2+ + 2H+ + H2O2 =2Fe3+ + 2H2O,故答案为:2Fe2+ + 2H+ + H2O2 =2Fe3+ + 2H2O;
Fe(SCN)3;②Fe2+被H2O2氧化生成Fe3+,从而增大Fe3+浓度,Fe3+、SCN-反应生成Fe(SCN)3,从而增大络合物浓度,溶液颜色加深,离子方程式为2Fe2+ + 2H+ + H2O2 =2Fe3+ + 2H2O,故答案为:2Fe2+ + 2H+ + H2O2 =2Fe3+ + 2H2O;
(5)根据①滴加FeCl3溶液无明显变化,说明SCN-发生了反应而不是Fe3+发生反应,滴加稀HCl和BaCl2溶液,产生白色沉淀,说明生成了硫酸根;根据②另取同浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化,说明O2不能氧化SCN-,所以氧化SCN-的为双氧水;故答案为:实验①说明SCN-发生了反应而不是Fe3+发生反应;实验②的目的是排除H2O2分解产生的O2氧化SCN-的可能;结论:H2O2将SCN-氧化成SO42—。

 名校课堂系列答案
名校课堂系列答案