题目内容
16.下列关于同系物的叙述不正确的是( )| A. | 同系物官能团的种类与个数必须相同 | |
| B. | 相邻两个同系物的相对分子质量相差14 | |
| C. | 通式相同的有机物一定互为同系物 | |
| D. | 同系物具有相似的化学性质 |
分析 A、官能团相同,且数目相同,结构相似,可为同一类有机物;
B、相邻两个同系物的相差一个CH2,相对分子质量相差14;
C、通式相同的有机物不一定是同系物,如甲醚与丙醇;
D、同系物结构相似,化学性质相似.
解答 解:A、官能团相同,且数目相同,结构相似,可为同一类有机物,故A正确;
B、相邻两个同系物的相差一个CH2,相对分子质量相差14,故B正确;
C、通式相同的有机物不一定是同系物,如甲醚与丙醇,故C错误;
D、同系物结构相似,分子相差若干个CH2,化学性质相似,故D正确;
故选C.
点评 本题考查了有机物的结构及性质、同系物的概念与辨析,题目难度不大,注意把握概念的内涵与外延,可以采用举例法来分析.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
6.下列化学用语表达正确的是( )
| A. | 醛基的结构简式:-COH | B. | 对硝基甲苯的结构简式: | ||
| C. | CH2F2的电子式: | D. | 乙烯的实验式:CH2 |
7.下列有关生活中化学的叙述,正确的是( )
| A. | 加碘食盐能使淀粉溶液变蓝 | |
| B. | 向水中通入O2,用以杀菌消毒 | |
| C. | 二氧化硅可用于制造半导体材料 | |
| D. | 向高硫煤中加入生石灰,可减少燃煤对大气的污染 |
1.甲、乙、丙三种含不相同离子的可溶性强电解质,它们所含的离子如下表所示:
若取等质量的甲、乙、丙配成相同体积的溶液,发现溶质的物质的量浓度c(甲)>c(乙)>c(丙),
则乙物质( )
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH-、NO3-、SO42- |
则乙物质( )
| A. | 可能是Na2S04 | B. | 可能是NH4NO3 | C. | 可能是NaOH | D. | 一定不是(NH4)2SO4 |
5.下列属于取代反应的是( )
| A. | 甲烷燃烧 | |
| B. | 在镍催化下苯与氢气反应生成环己烷 | |
| C. | 乙烯使溴水褪色 | |
| D. | 光照条件下甲烷与氯气反应生成一氯甲烷 |
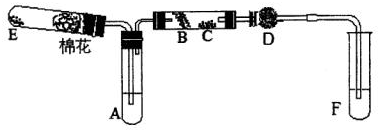
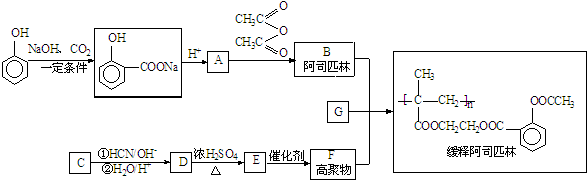
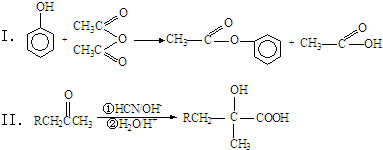
 ,写出E→F的反应类型加聚反应.
,写出E→F的反应类型加聚反应.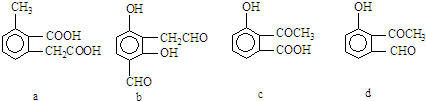
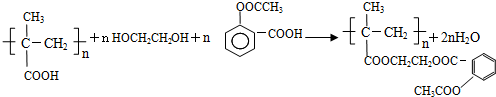 .
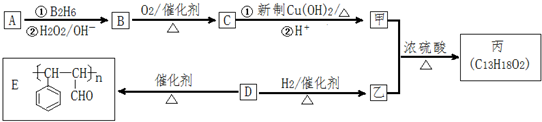
.
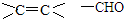 .
. (CH3)2CHCOONa+Cu2O↓+3H2O.
(CH3)2CHCOONa+Cu2O↓+3H2O.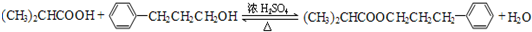 .
.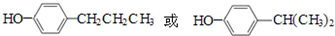 .
.