题目内容
7.下列有关生活中化学的叙述,正确的是( )| A. | 加碘食盐能使淀粉溶液变蓝 | |
| B. | 向水中通入O2,用以杀菌消毒 | |
| C. | 二氧化硅可用于制造半导体材料 | |
| D. | 向高硫煤中加入生石灰,可减少燃煤对大气的污染 |
分析 A.淀粉遇单质碘的溶液会变蓝;
B.氧气不具有杀菌消毒的作用,可以通入臭氧或氯气;
C.二氧化硅是光导纤维的主要成分,不能作半导体材料;
D.生石灰与煤中的硫燃烧生成的二氧化硫反应.
解答 解:A.淀粉遇单质碘的溶液会变蓝,而加碘食盐溶液中没有单质碘,不会变蓝,故A错误;
B.臭氧、氯气都具有强氧化性,向水中通入氯气或O3,可用以杀菌消毒,而氧气不能起到杀菌消毒的作用,故B错误;
C.用于半导体材料的是单质硅,而二氧化硅为光导纤维的主要成分,故C错误;
D.向高硫煤中加入生石灰,燃烧时可生成亚硫酸钙,可减少燃煤对大气的污染,故D正确;
故选D.
点评 本题考查了环境的污染与治理、硅和二氧化硅的性质等知识,题目难度中等,试题将化学性质与生活实际相结合,培养了学生灵活应用基础知识的能力,注意掌握常见元素单质及其化合物性质.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
19.已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp[Ag2CrO4(砖红色)]=9.0×10-12,下列说法不正确的是( )
| A. | 温度相同时,溶解度大小顺序为S(Ag2CrO4)>S(AgCl)>S(AgBr) | |
| B. | 往含Cl-,Br-,CrO42-浓度均为0.01mol•L-1溶液中滴加0.01mol•L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为Br-、CrO42-、Cl- | |
| C. | 用滴定法测KNO3溶液中KCl的含量时,可选择用AgNO3溶液做标准液,Ag2CrO4溶液做指示剂 | |
| D. | 1.88gAgBr投入到100mol/LNaCl溶液中有AgCl |
18.用括号内的试剂除去下列各物质中少量的杂质,正确的是( )
| A. | 溴苯中的溴(碘化钾溶液) | B. | 硝基苯中溶有NO2(氢氧化钠溶液) | ||
| C. | 乙醇中的乙酸(饱和碳酸钠溶液) | D. | 苯中的苯酚(溴水) |
15.对下列各有机物的叙述,正确的是( )
| A. | 蛋白质有多种生理功能,其水解的最终产物都是a-氨基酸 | |
| B. | 将溴乙烷与NaOH水溶液混合共热后加入足量硝酸酸化,再加入硝酸银溶液后会观察到淡黄色沉淀生成 | |
| C. | 取淀粉与稀硫酸共热后的溶液,加入新制的氢氧化铜悬浊液并加热,没有砖红色沉淀产生,说明淀粉尚未水解成葡萄糖 | |
| D. | 乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 |
2.已知甲醛(HCHO)分子中的4个原子是共平面的.下列分子中所有原子不可能同时存在于同一平面上的是( )
| A. | 苯乙烯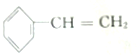 | B. | 苯甲酸 | C. | 苯甲醛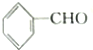 | D. | 苯乙酮 |
12.已知乙炔(C2H2)、苯(C6H6)、苯酚(C6H6O)的混合气体中含氢元素的质量分数为7%,则混合气体中氧元素的质量分数为( )
| A. | 83% | B. | 24% | C. | 68% | D. | 9% |
16.下列关于同系物的叙述不正确的是( )
| A. | 同系物官能团的种类与个数必须相同 | |
| B. | 相邻两个同系物的相对分子质量相差14 | |
| C. | 通式相同的有机物一定互为同系物 | |
| D. | 同系物具有相似的化学性质 |
17.一定温度下.将2molSO2和1molO2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol,当达到平衡状态时,下列说法中正确的是( )
| A. | 生成SO3 2mol | |
| B. | SO2和SO3物质的量之和一定为2mol | |
| C. | 反应放出197kJ的热量 | |
| D. | SO2的物质的量和SO3物质的量一定相等 |
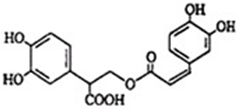 迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.请写出迭香酸中所有官能团的名称羧基、酯基、(酚)羟基、碳碳双键.
迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.请写出迭香酸中所有官能团的名称羧基、酯基、(酚)羟基、碳碳双键.